随着糖尿病患病率的持续上升,糖尿病伤口感染已成为临床面临的重大挑战。由于高血糖微环境和微血管功能障碍,糖尿病伤口易发生细菌感染,且愈合过程显著延迟。传统抗生素治疗面临耐药菌株(如耐甲氧西林金黄色葡萄球菌MRSA)的威胁,亟需开发新型无抗生素抗菌策略。活性氧(ROS)介导的化学动力疗法(CDT)和光动力疗法(PDT)展现出潜力,但CDT受限于糖尿病伤口中性至碱性的pH和不足的H2O2水平,而PDT依赖外部光源照射可能损伤正常组织。因此,构建一种无需外部光源、能够自适应调控伤口微环境的智能抗菌材料具有重要意义。

近日,武汉纺织大学青年教师胡烈锋和本科生王亚锾以共同第一作者在《Advanced Healthcare Materials》期刊上发表了题为“A Glucose-Fueled Metal-Organic Framework@Nanofiber Membrane Enables Self-Activated Chemodynamic-Photodynamic Therapy for Diabetic Infections”的研究论文。研究者通过静电纺丝技术结合Fe2+交联,成功制备了一种葡萄糖驱动的自激活MOF@纳米纤维复合膜(LPA@PHM(Fe))。该膜集成了PCN-222 MOF纳米光敏剂、原位生长的金纳米颗粒(Au NPs,具有葡萄糖氧化酶样活性)以及化学发光分子鲁米诺(Lum),封装于聚乙烯醇(PVA)和透明质酸(HA)构建的纳米纤维骨架中。该智能敷料可响应感染伤口中过表达的透明质酸酶和H2O2,触发MOF释放、局部葡萄糖消耗和pH降低,实现自供H2O2的增强型CDT,同时通过化学发光共振能量转移(CRET)激活PDT,无需外部光源。
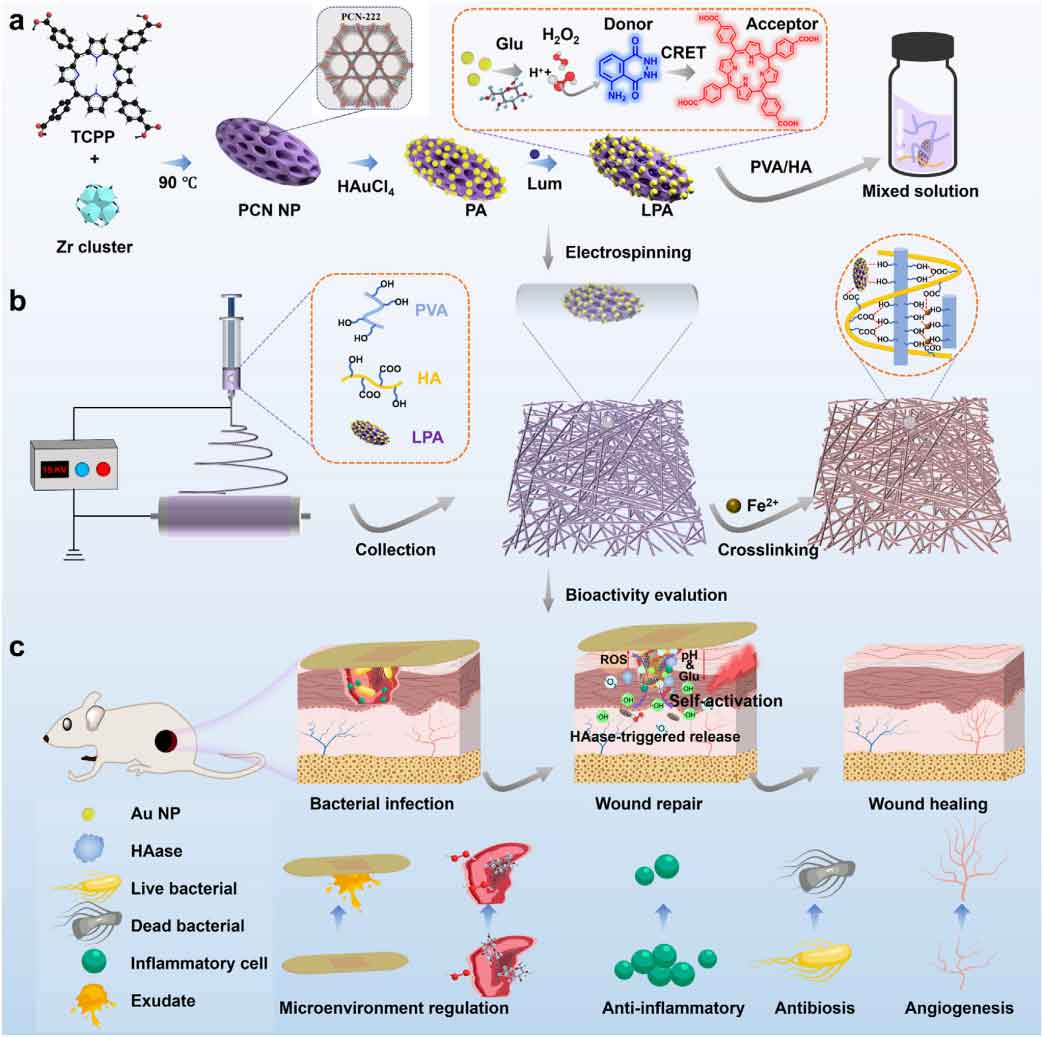
图1:LPA@PHM(Fe)纳米纤维复合膜的制备及其在糖尿病感染伤口愈合中的作用机制示意图。
研究者首先合成了梭形PCN-222 MOF纳米颗粒,并在其表面原位生长Au NPs,随后物理包封鲁米诺分子,得到LPA复合纳米颗粒。通过静电纺丝将LPA均匀负载于PVA/HA纳米纤维膜中,再利用Fe2+进行交联,最终获得LPA@PHM(Fe)复合膜。透射电镜(TEM)和能谱分析(EDX)证实了Au NPs在MOF表面的均匀分布以及Lum的成功负载。X射线衍射(XRD)和氮气吸附-脱附等温线表明,LPA保留了PCN-222的晶型结构和介孔特性,同时比表面积略有下降,证实了Au和Lum的引入。
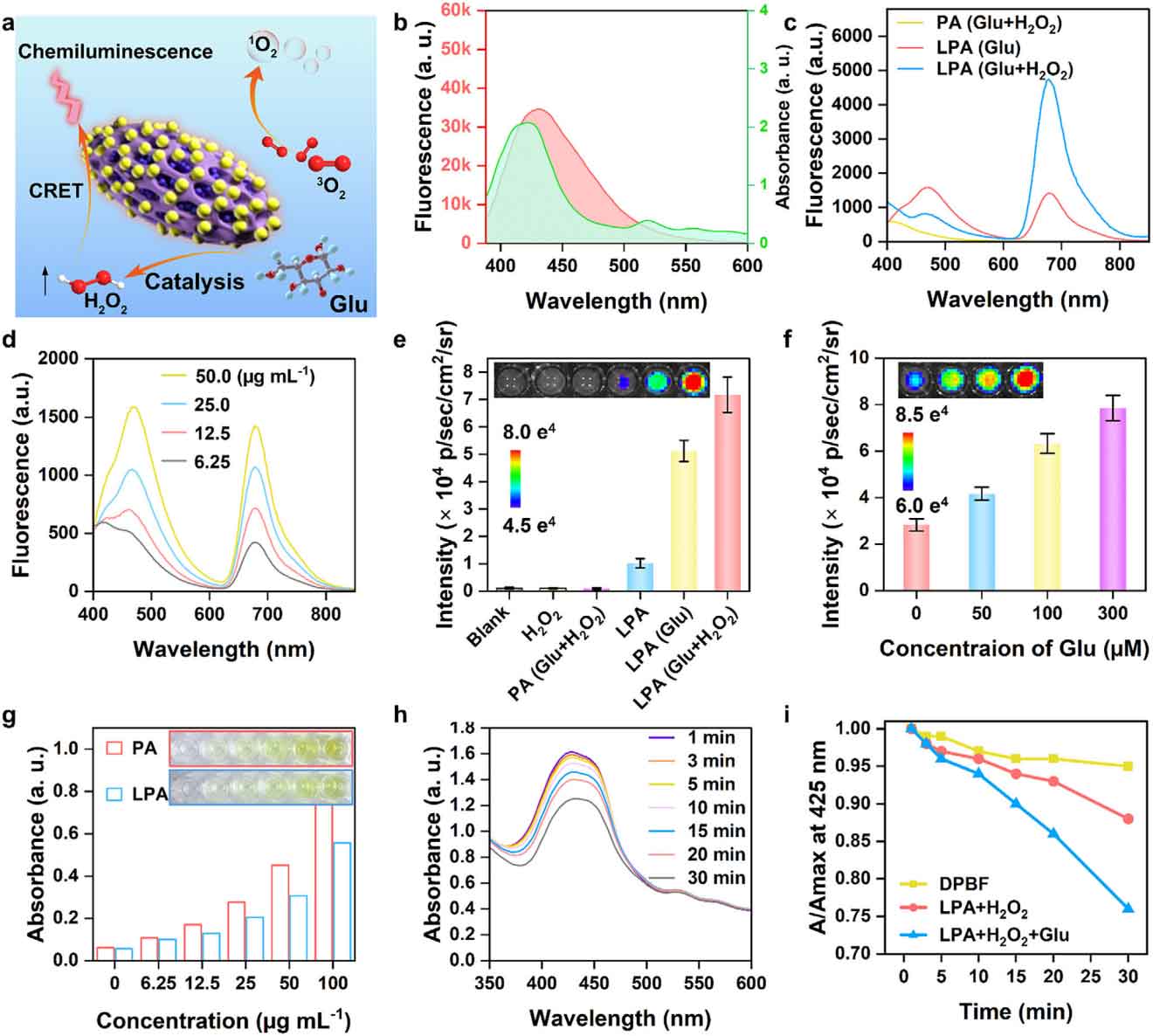
图2:LPA介导的CRET过程及其光敏性能。
UV-vis光谱和发光光谱证实,PCN-222的吸收峰(约410 nm)与Lum的化学发光发射峰(约425 nm)高度重叠,CRET效率高达78.3%。在100 μM H2O2(模拟慢性伤口内源浓度)存在下,LPA NPs表现出浓度依赖性的强化学发光,且添加葡萄糖(20 mM)后发光强度进一步提升,归因于Au NPs催化葡萄糖产生额外H2O2。DPBF探针实验表明,LPA+H2O2+Glu组在无外部光照下显著产生1O2,证明该体系实现了自激活PDT。
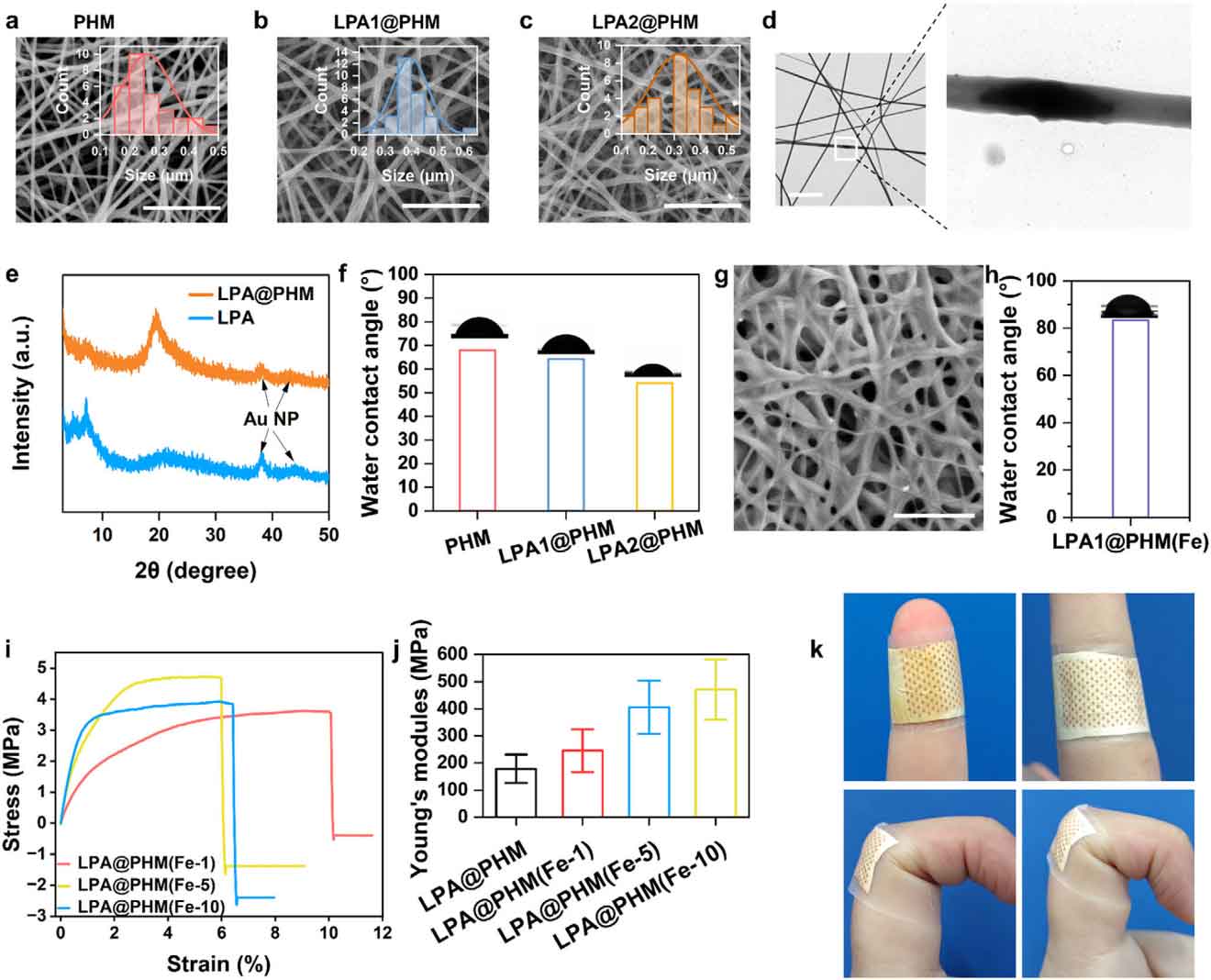
图3:复合纳米纤维膜的表征。
SEM和TEM显示,LPA NPs均匀嵌入并沿纤维轴向排列,未破坏纳米纤维的多孔结构。水接触角测试表明,LPA的引入增强了膜的亲水性(接触角从68°降至54°)。Fe²⁺交联后,膜的水接触角升至83.4°,但仍保持亲水特性,同时杨氏模量显著提高,机械强度增强。该膜可轻松集成于绷带模型中,贴合皮肤并保持结构完整性。
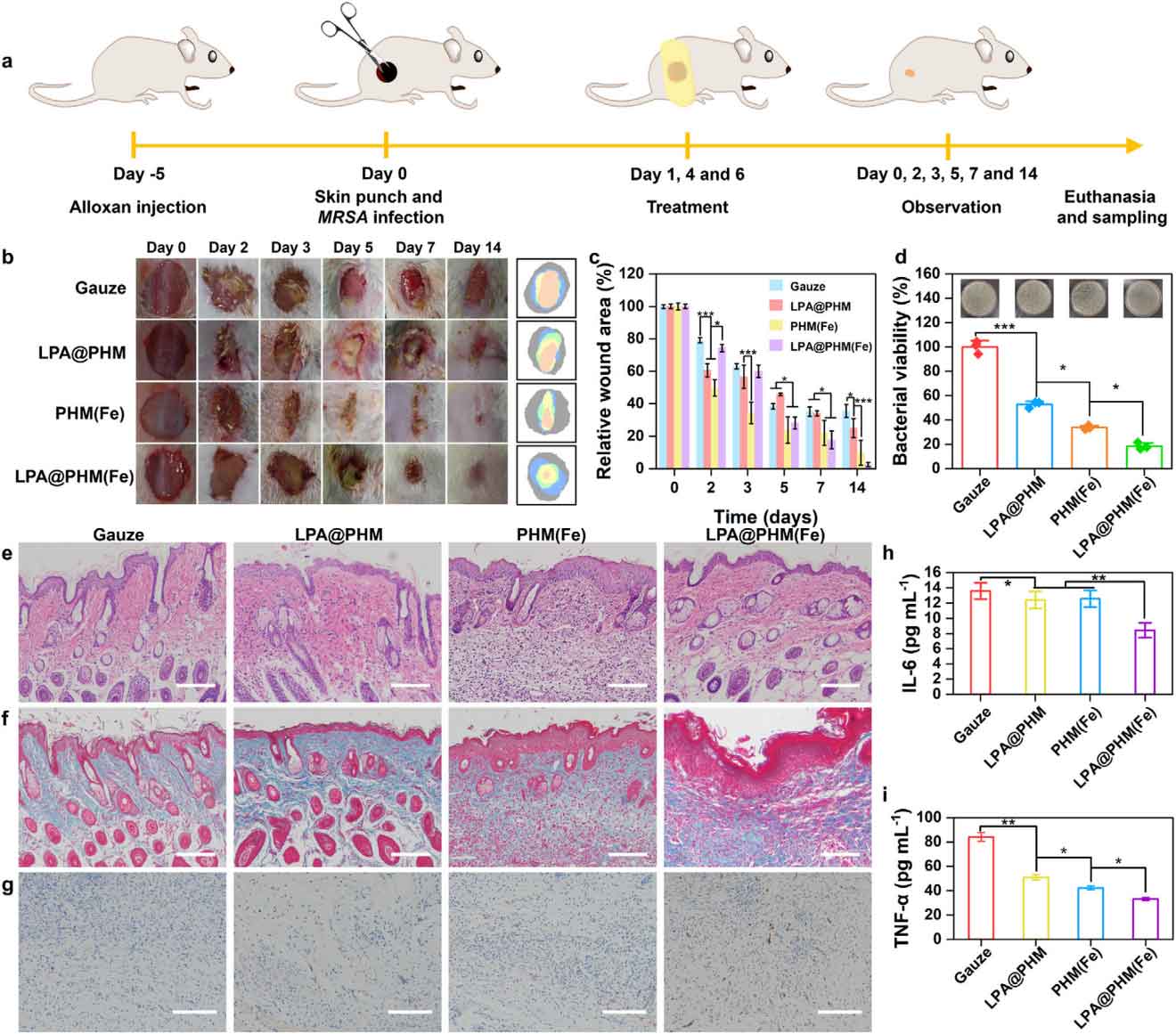
图4:LPA@PHM(Fe)加速糖尿病MRSA感染伤口愈合的体内评价。
在糖尿病小鼠MRSA感染全层皮肤缺损模型中,LPA@PHM(Fe)组在第14天实现完全伤口闭合,而对照组仍有明显溃疡。伤口细菌计数显示,LPA@PHM(Fe)组菌落数最低,抗菌效果显著。组织学分析表明,该组再生皮肤具有完整的毛囊结构、致密的胶原沉积(Masson染色蓝色最深)和丰富的CD31阳性新生血管。血清炎性因子(IL-6、TNF-α)水平显著降低,且主要器官未见明显毒性,生物相容性良好。
综上,该研究通过静电纺丝技术成功构建了一种葡萄糖驱动的自激活MOF@纳米纤维复合膜,实现了无需外部光照的CDT/PDT协同抗菌治疗。该智能敷料能够响应感染微环境,自主调控葡萄糖、pH和H2O2水平,为糖尿病感染伤口的无抗生素治疗提供了新策略,在可穿戴医疗和智能伤口敷料领域具有广阔的应用前景。
论文链接:https://doi.org/10.1002/adhm.202600123
人物简介:
胡烈锋,武汉纺织大学生物工程与健康学院(生康学院)讲师,硕士生导师。2022年毕业于武汉大学药学院,主要研究方向包括:智能药物递送技术开发、多功能纳米材料设计及其生物医学应用基础研究,以及代谢产物精准分析与靶点药物开发。近年来,以第一作者或通讯作者身份在 Chemical Engineering Journal、Journal of Nanobiotechnology、Advanced Healthcare Materials、Science China Materials等期刊发表论文10余篇;申请中国专利2项,其中授权1项;参与国家自然科学基金面上项目和联合基金项目各1项。
