随着烧伤创面治疗需求的不断增加,如何实现生长因子的稳定递送和高效局部修复,已成为生物材料与再生医学领域的重要研究方向。酸性成纤维细胞生长因子(aFGF)能够促进细胞增殖、迁移、胶原沉积和血管生成,在烧伤修复中具有良好应用前景。然而,aFGF 作为蛋白类生物活性分子,易受温度、pH、酶降解和氧化等因素影响而失活,且在创面局部难以维持有效浓度。因此开发安全、温和且可控的蛋白递送系统具有重要意义。

近日,沈阳药科大学杨明世教授/郭雄副教授/寸冬梅教授团队在期刊《Journal of Nanobiotechnology》发表了题为“Ionic-bridge engineered α-lactalbumin nanoparticles integrated into electrospun nanofibers for controlled growth factor delivery and burn wound repair”的最新研究成果。研究者提出一种无需交联剂的α-乳清蛋白(ALA)纳米颗粒构建策略,通过 Ca²⁺ 介导的“离子桥”作用,将 ALA工程化为纳米颗粒,并包载 aFGF 形成 aFGF@ALA 纳米颗粒。随后,研究者一步将该纳米颗粒整合进聚乙烯醇(PVA)静电纺丝纳米纤维中,构建出兼具结构支撑与控释能力的复合敷料(aFGF@ALA NPs/PVA ENMs)。
该复合体系将纳米颗粒的生物活性递送能力与纳米纤维的物理支撑和创面覆盖功能相结合,形成了“颗粒控释 + 纤维支撑”的协同治疗平台。结果表明,该材料能够有效保护 aFGF 的生物活性,实现持续释放,并显著促进成纤维细胞和角质形成细胞的增殖与迁移。在深度烧烫伤大鼠模型中,aFGF@ALA NPs/PVA ENMs能明显加速创面愈合,促进再上皮化、胶原 I/III 重塑和血管生成,展现出良好的烧伤修复效果。这项工作为生长因子的递送和创面修复材料设计提供了一种简便、温和且具有推广潜力的新策略。
研究者利用 Ca²⁺ 与 ALA 分子中阴离子基团之间的相互作用,在水相环境中形成稳定的“离子桥”,从而诱导 ALA 组装成纳米颗粒。相比传统交联剂法,该策略更加温和、安全,适合生物活性蛋白的加工。进一步结合电喷雾技术,成功获得粒径均一、形貌稳定的 aFGF@ALA 纳米颗粒。
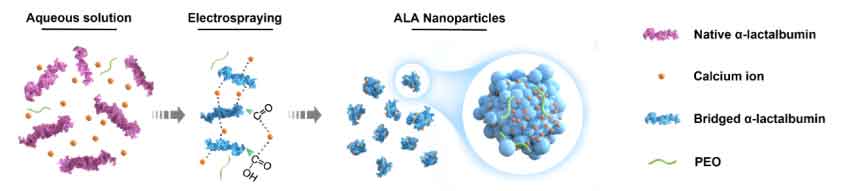
图1:基于“离子桥”策略构建ALA纳米颗粒过程。
研究者将制备好的 aFGF@ALA 纳米颗粒整合进 PVA 静电纺丝纳米纤维中,形成复合纳米纤维膜。该材料兼具高孔隙率、良好柔性和仿生细胞外基质结构,同时可实现 aFGF 的持续释放,从而为创面修复提供更持久的生物活性支持。
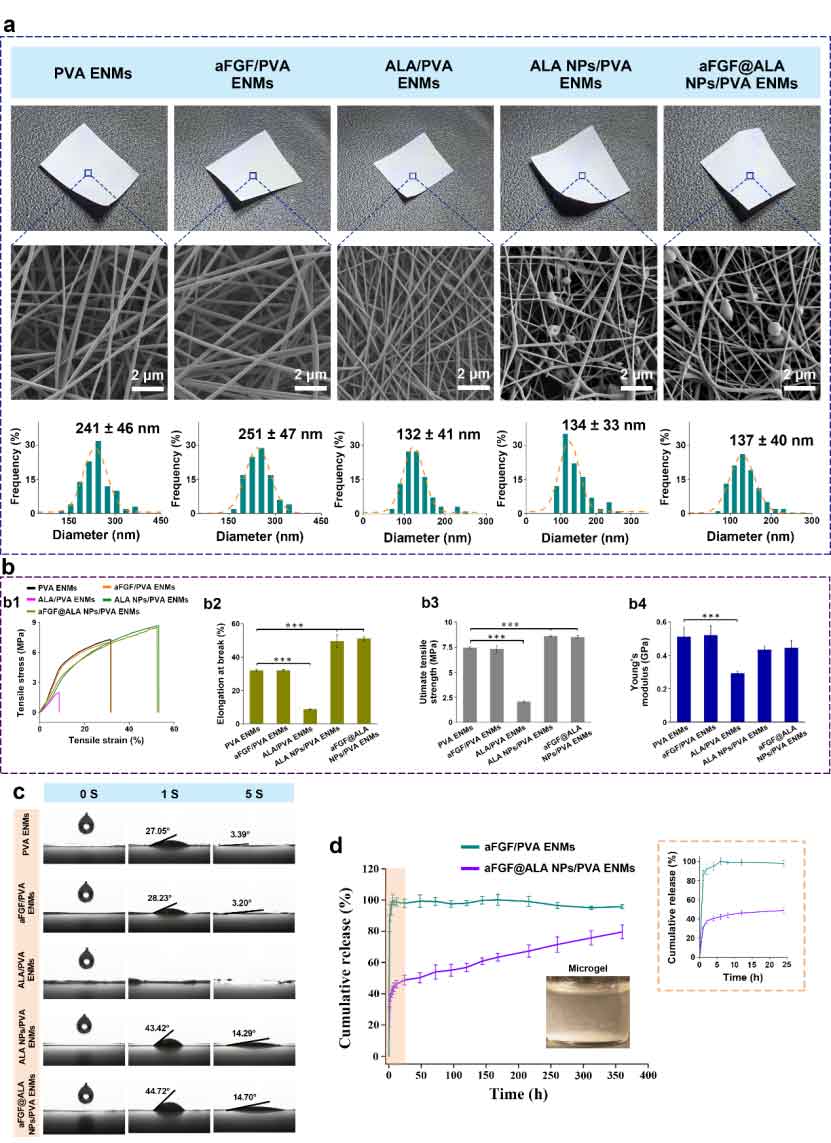
图2:aFGF@ALA NPs/PVA ENMs 的构建与结构特征。
实验结果显示,该复合敷料能够显著促进成纤维细胞和角质形成细胞的增殖、迁移,说明其不仅具有良好的细胞相容性,载体蛋白ALA还能够主动参与创面修复过程,提升组织再生效率。
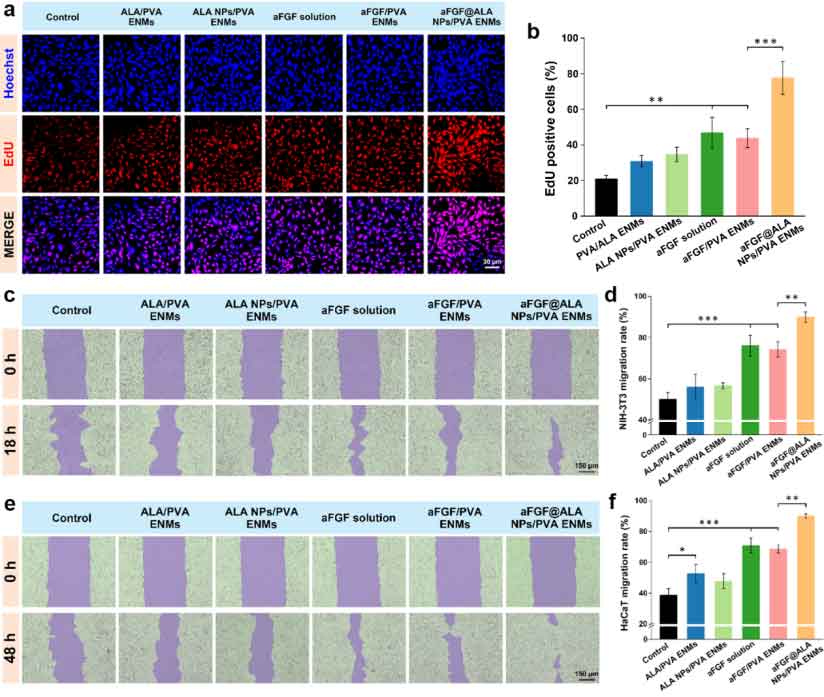
图3:体外细胞实验表明材料具有良好生物相容性和促修复能力。
在深度烧伤大鼠模型中,aFGF@ALA NPs/PVA ENMs 显著加快了创面闭合和再上皮化进程,并促进胶原沉积、胶原重塑及血管生成,表现出优异的烧伤创面修复能力。
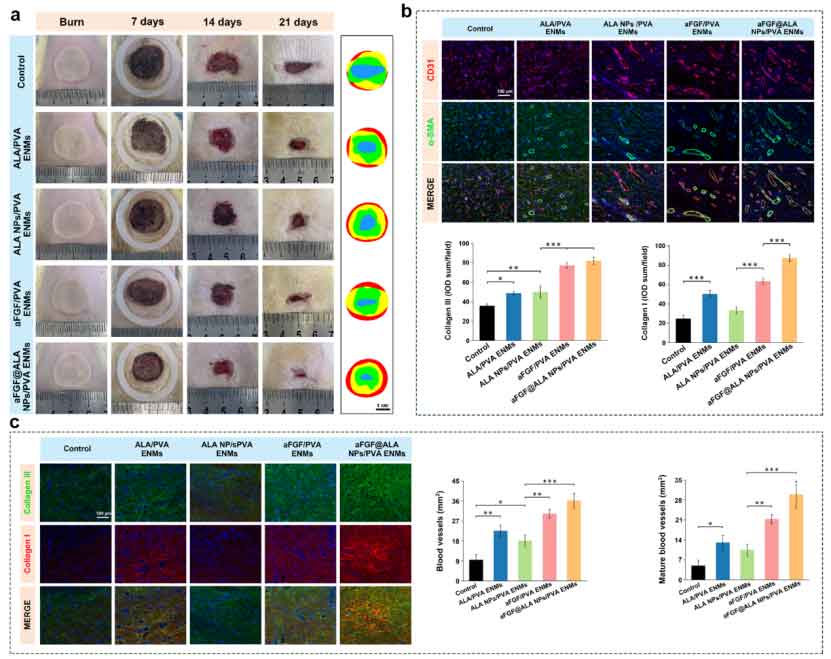
图4:体内深度烧伤模型验证了材料的修复效果。
总体来看,该研究通过“离子桥”工程化ALA蛋白纳米颗粒,并将其与静电纺丝纳米纤维结合,构建出一种具有控释、生物稳定性和组织修复促进功能的复合敷料。该策略不仅为 aFGF 的局部递送提供了新的、且有效平台,也为生长因子在组织修复中的应用提供了新的材料思路。
论文链接:https://doi.org/10.1186/s12951-026-04393-3
