周围神经的电调节和修复依赖于高质量的组织-生物电子接口。然而,当前的导电材料通常表现出不稳定的导电性、机械错配和有限的加工性,这会影响其支持结构再生和长期神经调节的能力。

针对上述挑战,北京化工大学薛佳佳教授团队开发了一种基于电活性核壳纳米纤维的柔性生物电子界面,用于周围神经修复与在体神经调控。该平台通过一步同轴静电纺丝技术,将具有力学顺应性的聚己内酯(PCL)核心与双连续导电聚(3,4-乙烯二氧噻吩):聚苯乙烯磺酸盐/聚氨酯(PEDOT:PSS/PU,简称PPP)壳层相结合,使支架兼具稳定的本征导电性、匹配神经组织的力学性能和良好的加工性。该纳米纤维既可组装为柔性神经生物电极,实现高效神经刺激与高保真电生理记录,同时又能作为神经导管,通过拓扑引导与局部电调节的协同作用,显著促进轴突伸长、髓鞘再生与运动功能恢复,其修复效果接近自体神经移植。相关论文以“Nanofiber-Based Electroactive Interfaces Enabling Coordinated Neuromodulation and Peripheral Nerve Regeneration”为题,发表在《Advanced Materials》上。
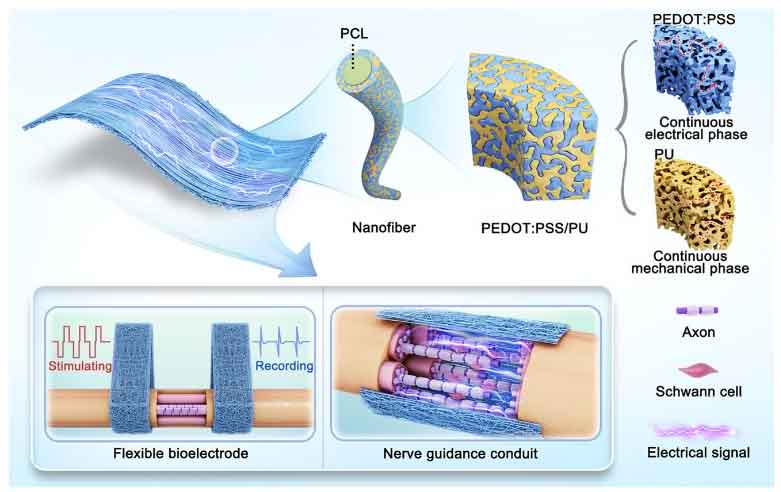
图1. 电活性核壳纳米纤维的制备与应用示意图。
研究团队首先对PPP双连续结构的形成参数进行了系统优化。通过调控乙醇/水混合溶剂比例及PEDOT:PSS与亲水性PU的质量比,发现在70 vol%乙醇及30/70的配比下,可形成兼具连续导电网络与力学网络的理想双连续结构。该组分下制备的PPP薄膜在生理相关水合状态下,电导率达77.1 ± 11.6 S m⁻¹,断裂伸长率高达199%,模量(3.0 ± 0.4 MPa)与周围神经组织(5-14 MPa)高度匹配,有效克服了PEDOT:PSS本身脆性高的缺点。基于此优化配方,通过一步同轴静电纺丝成功制备了PCL/PPP核壳纳米纤维。通过调节收集辊转速,可构建内层高度取向、外层随机排列的双层支架。
所有纤维(PCL, PCL/3%PPP, PCL/5%PPP, PCL/7%PPP)均呈现均一无珠串的形貌,平均直径在240-264 nm之间,透射电镜(TEM)清晰证实了其核壳结构。重要的是,PCL/PPP纳米纤维支架在保持良好亲水性与力学柔顺性的同时,电导率(PCL/3%PPP组为2.36 ± 0.66 S m⁻¹)比纯PCL高出三个数量级,且能稳定维持一个月以上。电化学阻抗谱(EIS)显示其界面阻抗(约40 kΩ)显著低于纯PCL(约70 kΩ),循环伏安(CV)与电荷注入容量(CIC)测试也证实其具备更优的电荷存储与安全刺激能力,甚至可直接点亮LED灯,展现了其作为柔性神经界面的巨大潜力。
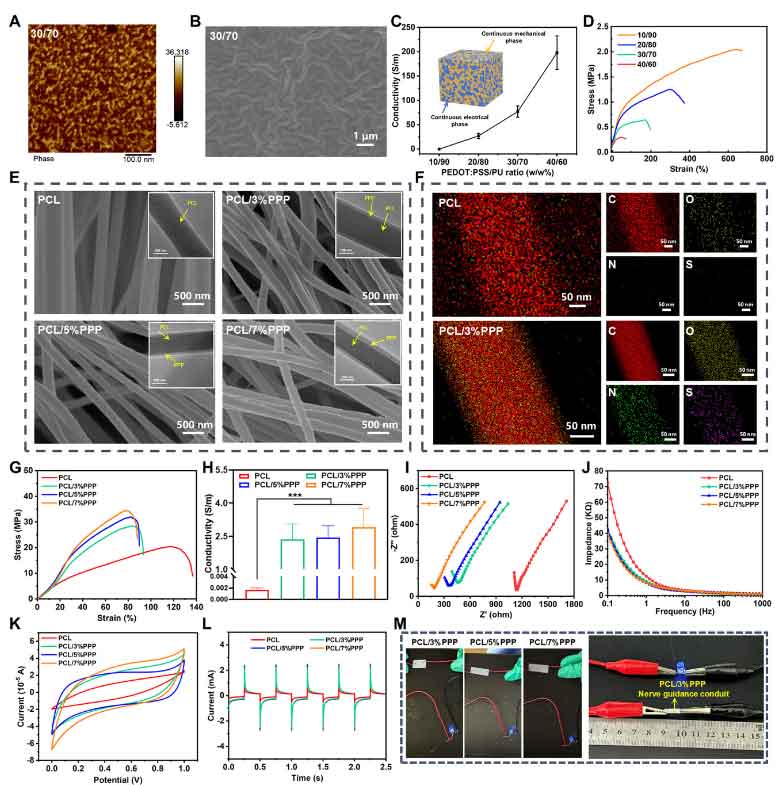
图2. 电活性纳米纤维的物理与电化学表征。
在体外细胞实验中,研究者评估了支架对SCs与神经元的影响。SCs培养结果显示,PCL/3%PPP支架显著促进了细胞的伸长与极化,细胞突起长度较纯PCL组增长近2倍,并显著上调了髓鞘相关基因(PMP22, Krox20, NGF)的表达。细胞内钙离子(Ca²⁺)成像揭示,电活性界面能够维持SCs更低的细胞内钙水平,这有助于通过抑制CaSR-PLC信号通路,解除PKC对髓鞘形成基因的抑制,从而促进髓鞘形成。在背根神经节(DRG)和PC12细胞模型中,PCL/3%PPP支架同样展现了最强的促轴突伸长能力,平均轴突长度分别是纯PCL组的2.2倍(DRG)和1.7倍(PC12细胞),并显著上调了神经成熟与轴突生长相关基因(GAP-43, NF-H, NF-L, Synapsin I, PSD-95)的表达。这些结果共同表明,适度引入导电相(3% PPP)能最有效地促进SCs髓鞘化及神经元轴突生长,而过高的导电组分则可能因细胞相容性下降而削弱该效应。
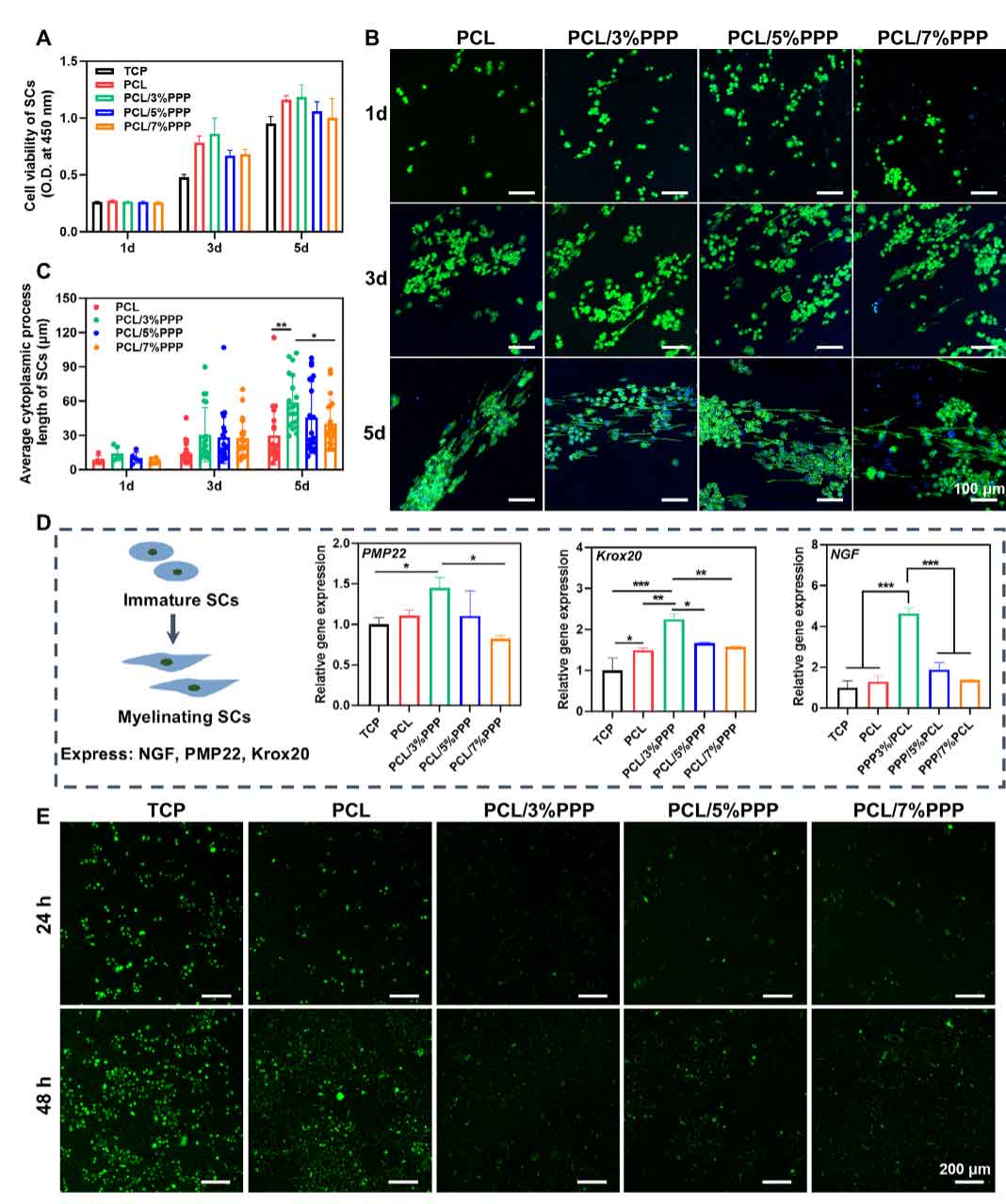
图3. 电活性纳米纤维促进施万细胞(SCs)增殖和髓鞘形成。
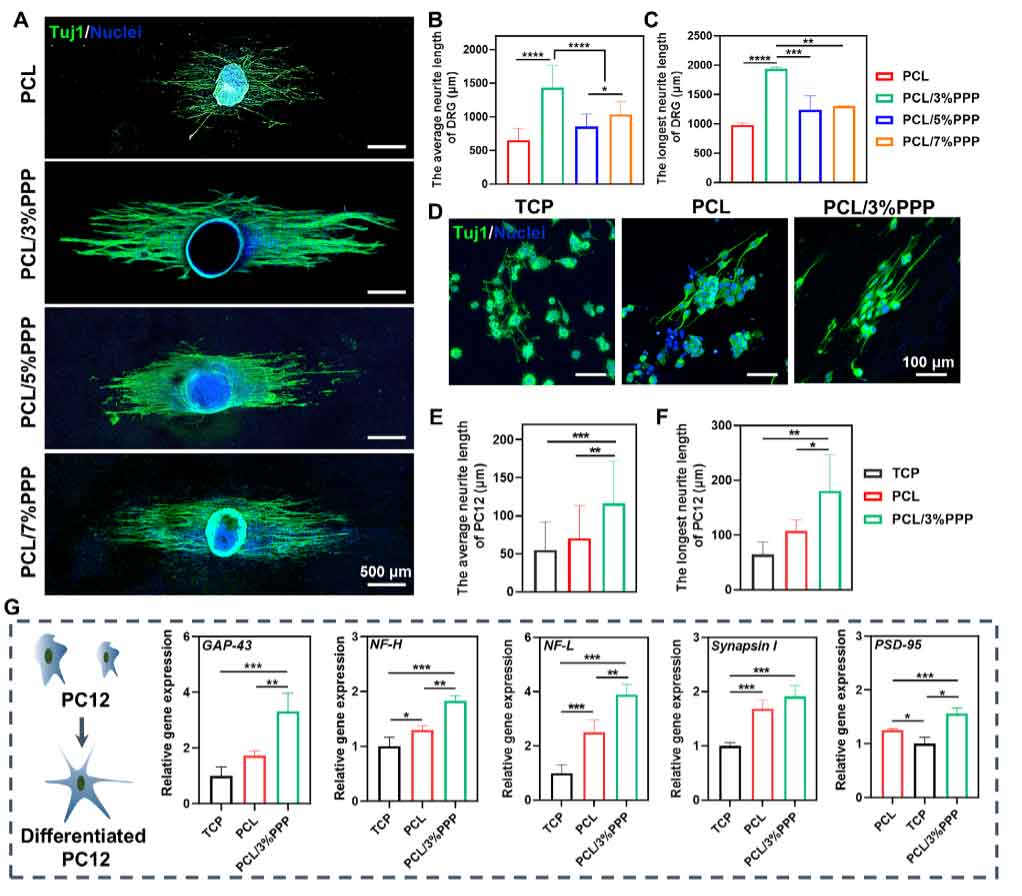
图4. 电活性纳米纤维促进轴突延伸。
为了验证其在体功能性,研究者将PCL/3%PPP纳米纤维支架作为柔性生物电极,在大鼠坐骨神经和恒河猴正中神经上进行电刺激并记录复合肌肉动作电位(CMAP)。结果表明,在相同刺激参数下,该柔性电极引发的踝关节旋转角度、CMAP波幅及潜伏期与临床使用的刚性铜针电极相比均无统计学差异,证实了其高效的神经电耦合能力。尤为重要的是,柔性纤维电极在接触神经表面后未留下任何压痕或组织损伤,而刚性金属电极则造成了明显的局部压迫。这凸显了其通过降低机械失配,减少界面应力与组织创伤,从而在长期植入中减轻炎症与纤维化包裹的潜力。
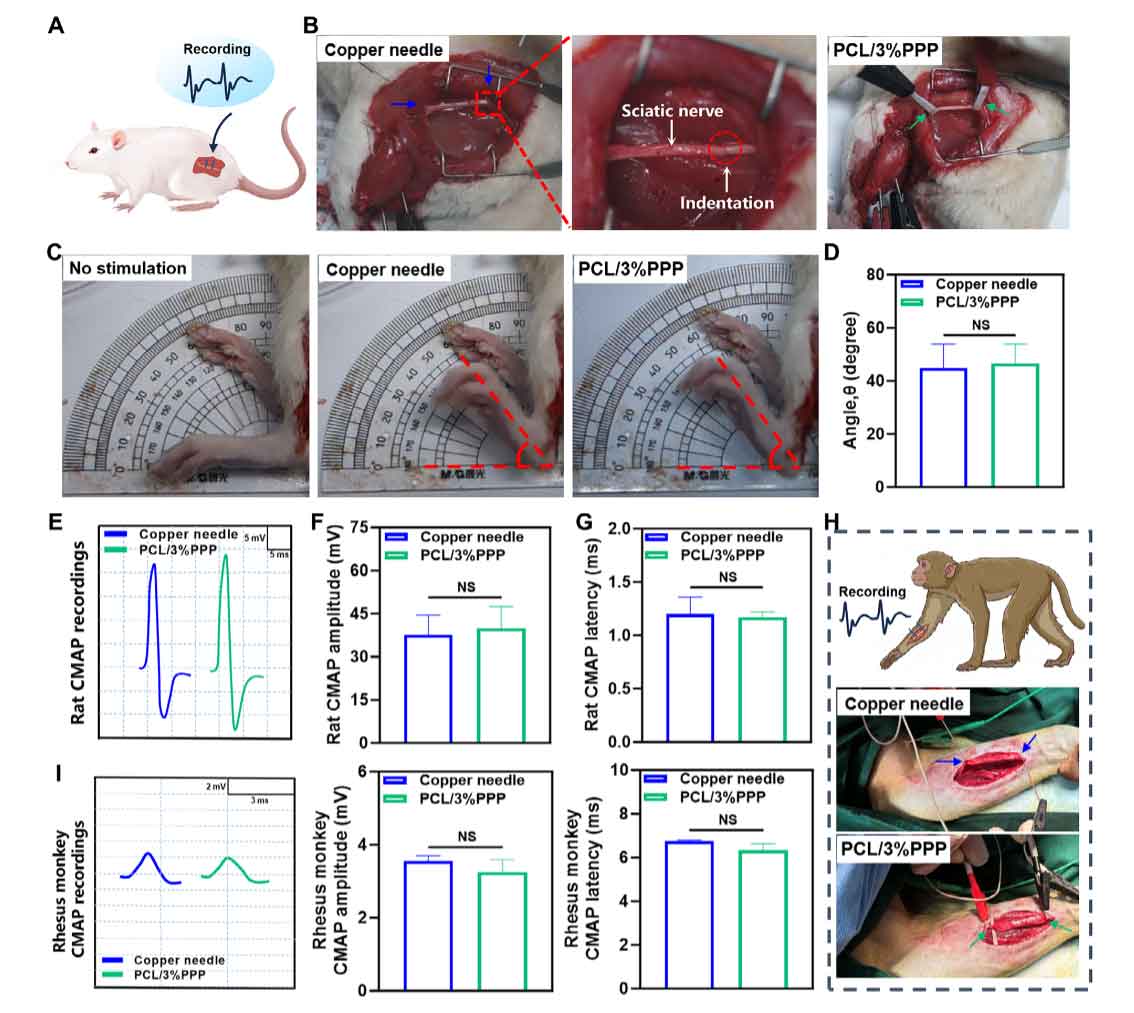
图5. 电活性纳米纤维在体神经刺激与同步CMAP记录。
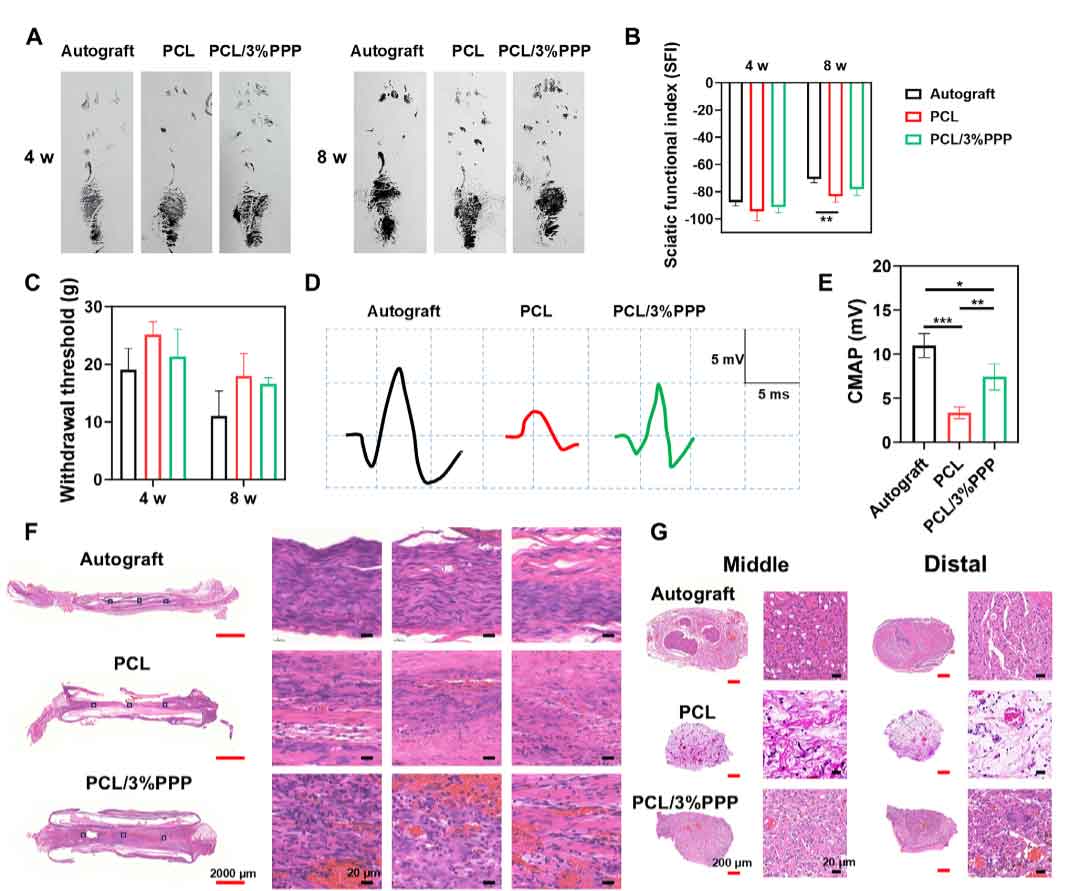
图6. 再生坐骨神经的功能与形态学评估。
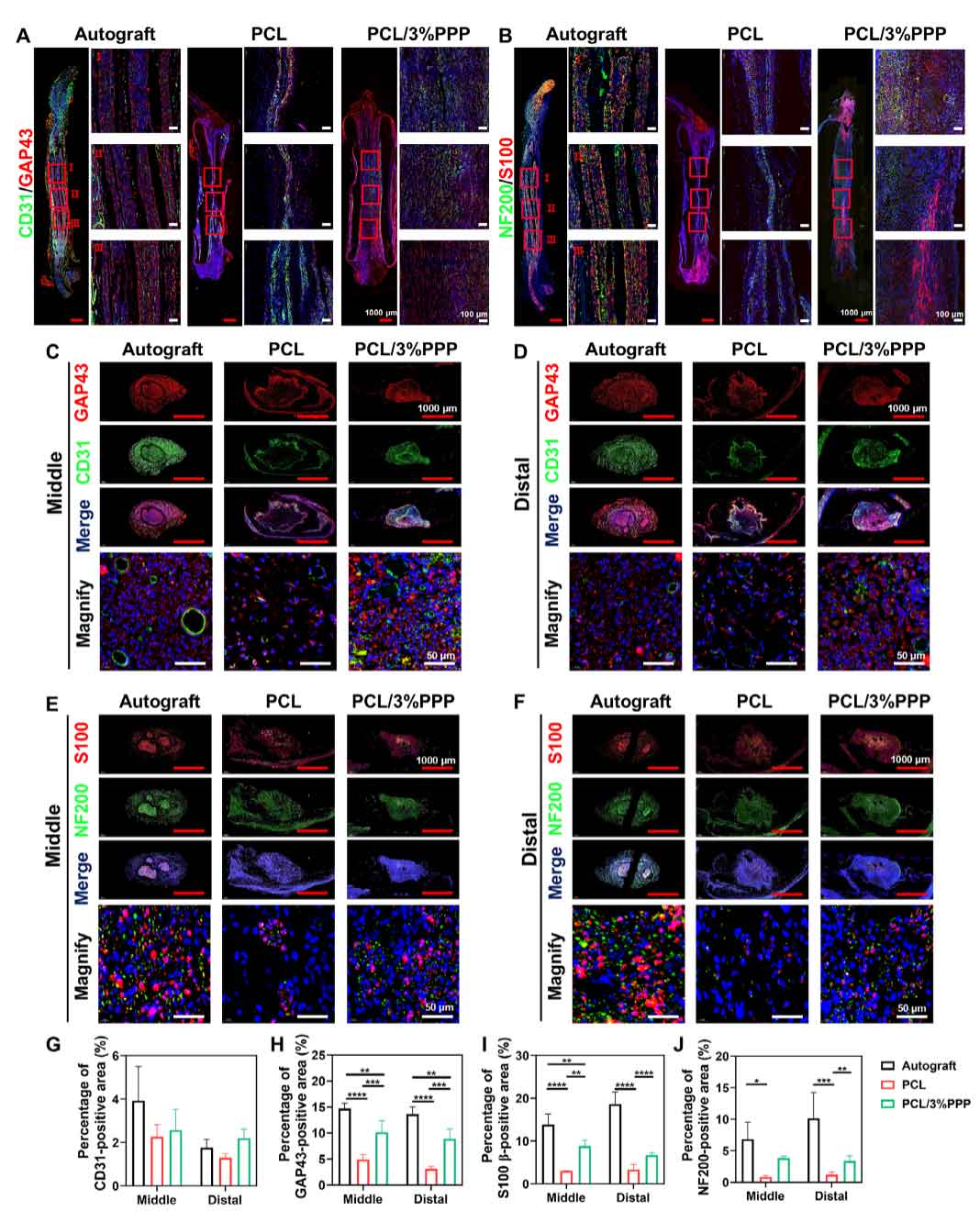
图7. 再生神经的免疫荧光染色。
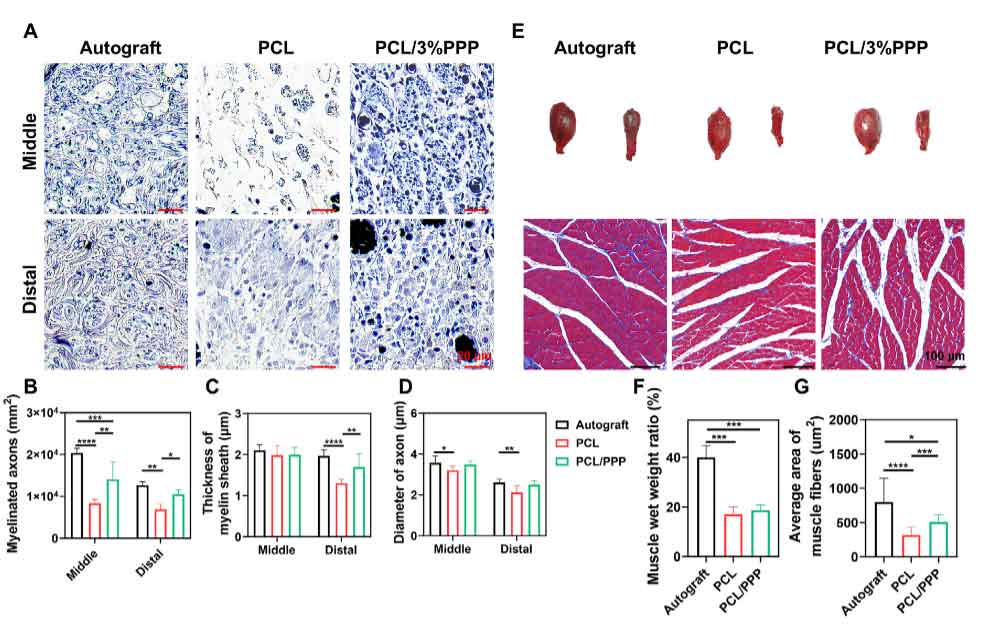
图8. 髓鞘再生与腓肠肌恢复评估。
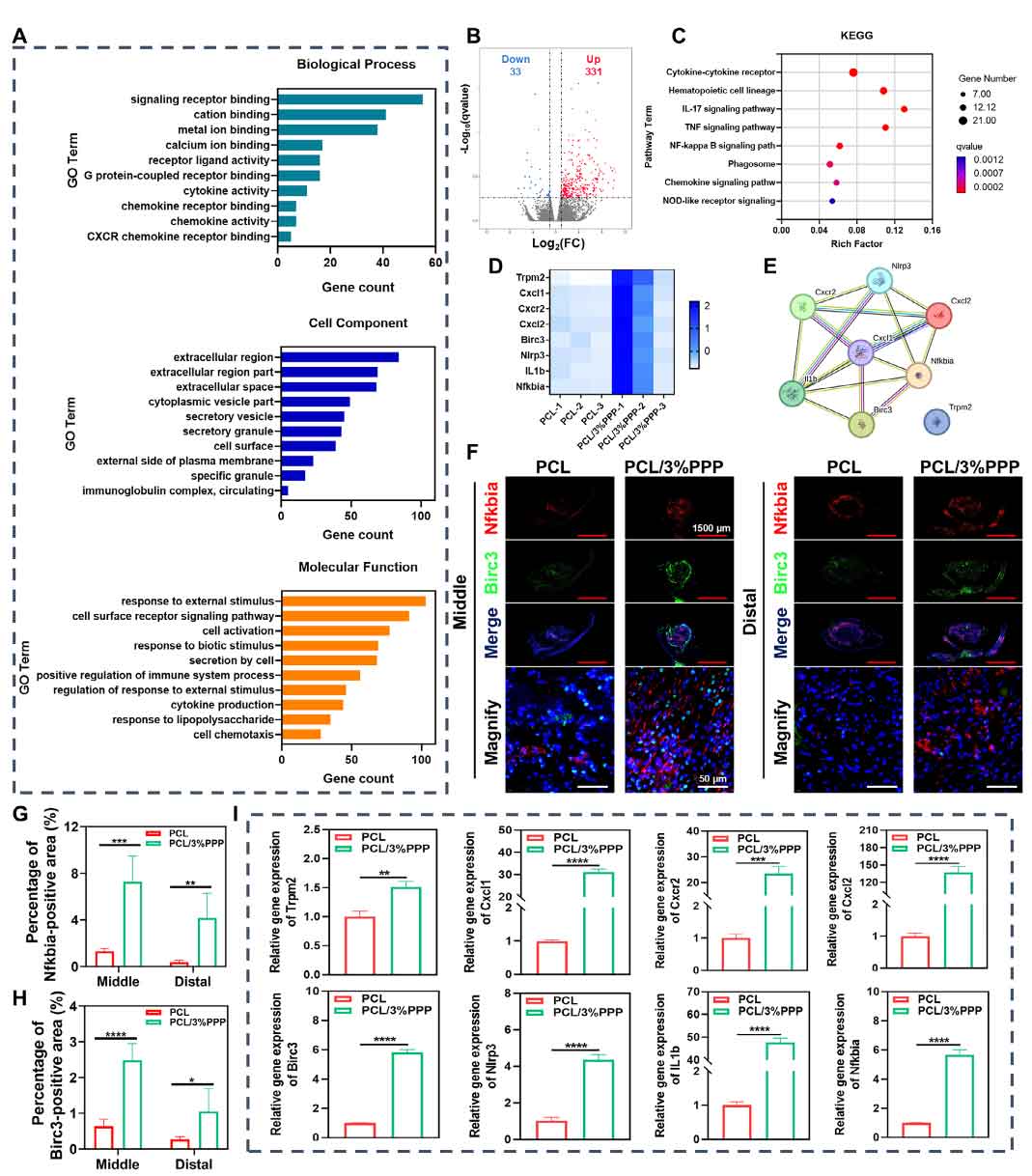
图9. 转录组分析揭示电学信号介导的再生通路激活。
结论
本研究开发的一体化PCL/PPP核壳纳米纤维支架,成功地将柔性神经界面与功能性神经再生两大功能融合于同一平台。该支架不仅具备优异的导电性、力学顺应性和可加工性,更能通过其本征的电活性协同拓扑引导,在无需外源性电刺激或生物活性因子的情况下,有效促进施万细胞髓鞘化、轴突伸长、血管新生和运动功能恢复,其修复效果直逼自体神经移植。该工作为下一代生物电子支架的设计提供了新思路,通过精确协调神经调控与结构修复,为周围神经损伤乃至其他神经退行性疾病的治疗开辟了新的途径。未来,通过进一步优化支架降解动力学、集成无线模块以实现无束缚操作,该平台将具有广阔的临床转化前景。
原文链接: https://doi.org/10.1002/adma.72880
