
可穿戴表皮监测在健康评估中具有重要意义。然而,目前的电子皮肤受到汗液堆积导致的一致性差、低透气性带来的不适以及信号单一的限制,使得长期、稳定、高通量的信号记录变得非常困难。
基于此,中山大学周建华教授、乔彦聪副教授与清华大学任天令教授合作,在《Nano-Micro Letters》期刊上发表了题目为“An Integrated Flexible Bioelectrical and Biochemical Monitoring System Based on Spindle-Structured Directional Sweat-Pumping Nanomesh”的论文。该研究中,作者采用静电纺丝技术制备一种纺锤结构定向吸汗纳米网(SDSN)。通过结合多种不对称性,包括润湿性、孔径和纺锤结结构,SDSN建立了协同力,使液体单向输送的速度比人类运动时的排汗速度快1000倍以上。为了体现流体导向的优势,构建了双结构、双视角的比较模型框架。引入Au 纳米网作为电极允许Au 纳米网电极同时监测电化学和电生理信号,同时保持良好的皮肤顺应性和运动稳定性。此外,还研制了一种纳米网格封装柔性电路,实现了连续无线监测。该系统显示了代谢能量输出与心血管反应相关性分析的潜力,使其成为高强度体力劳动和运动期间健康管理的理想工具。
本文亮点:
通过控制静电纺丝,纳米网集成了润湿性和结构梯度,实现了超快的单向液体输送,速度高达4.00 mL min-1 cm-2。
设计了具有高透气性和透湿性的金纳米电极,为运动过程中稳定的皮肤监测提供了优越的一致性和拉伸性,同时具有出色的皮肤相容性。
该系统可以实现无线和连续的电化学和电生理监测,结合汗液生物标志物和心电图信号进行全面的健康分析。
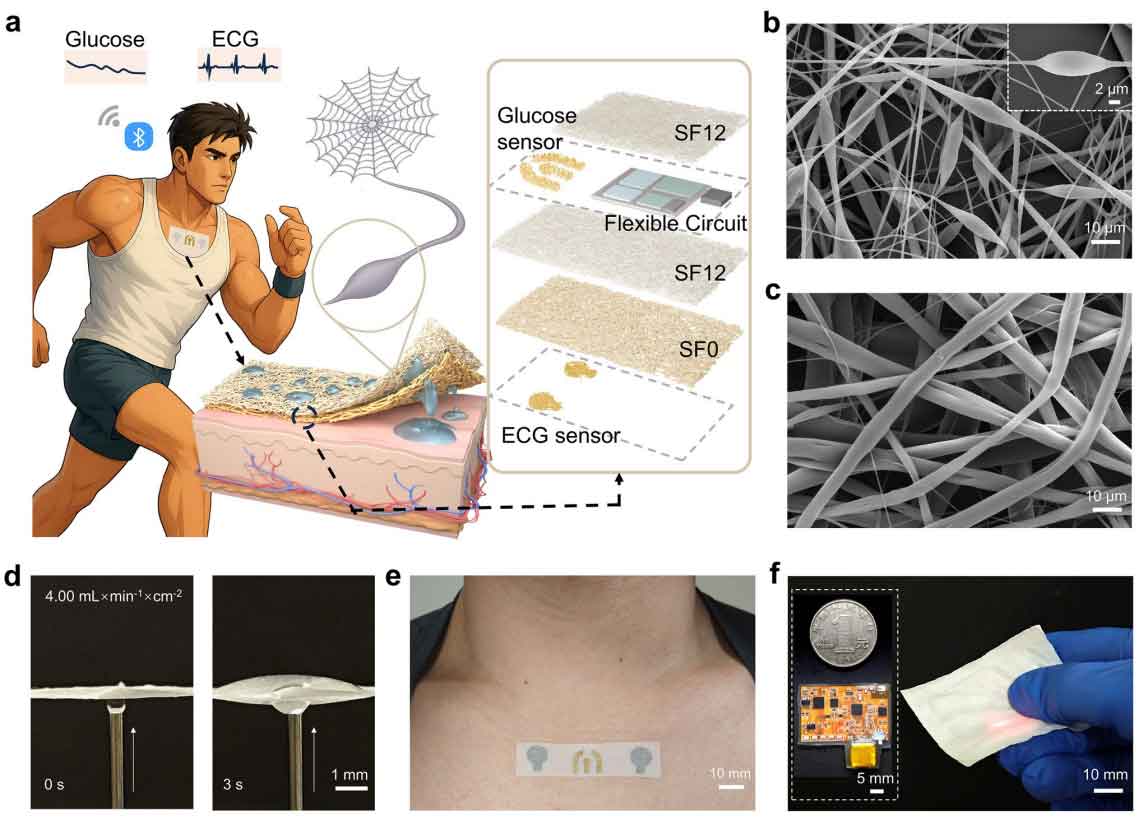
图1 一种具有定向汗液输送的纺锤结构纳米网柔性系统,用于综合生物电和生化监测。
集成多模态系统的设计
SDSN作为核心功能层,实现单向汗液输送。在SDSN内部形成密集均匀分布的纺锤结结构。如图1b、c所示,两层SDSN具有不同的形貌:亲水性SF12层具有较小的孔和周期性的纺锤结,而疏水性SF0层由更厚、更均匀的纳米纤维组成,形成较大的孔。当液体从疏水侧引入时,它被迅速向上泵送并保留而没有回流(图1e)。该集成系统专为胸部安装应用而设计,这是临床上首选的心电测量位置,可确保高信号质量,同时减少运动伪影(图1e)。该系统进一步集成了纳米网格封装的检测电路和无线传输模块(图1f),保持了系统的整体透气性和水蒸气透射率。
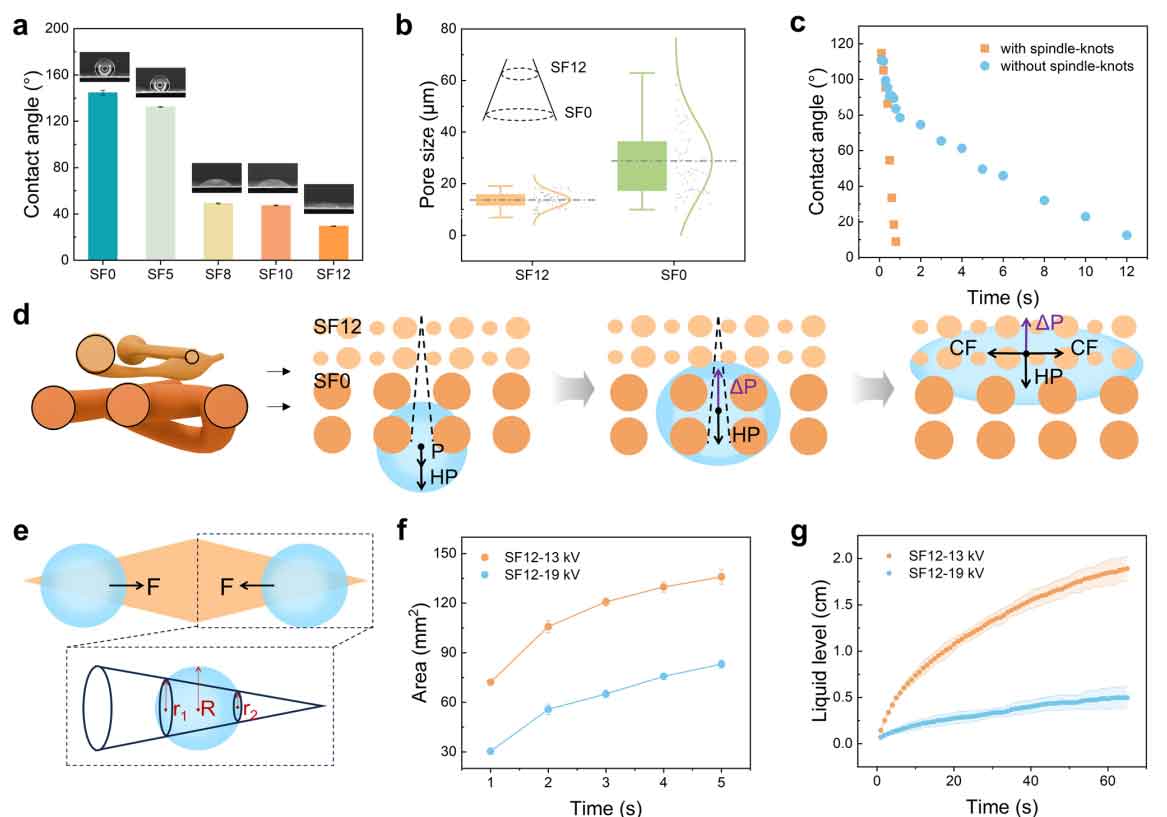
图2 SDSN设计及液体输运特性。
纺锤结构定向导汗纳米网的设计
该研究制备了 SF0–SF12 系列配方,亲水性随 F127 含量增加单调提升(图 2a),静态水接触角从 144°(SF0)降至 29.5°(SF12)。据此,将 SF12 作为亲水性层、SF0 作为疏水性层,构建出所需的Janus 润湿性梯度。
纳米网的孔径与纺锤结结构可通过系统调控静电纺丝参数(针头内径、施加电压、推进速度)进行定制。与 SF12 相比,SF0 的平均孔径更大,从而形成锥形通道(图 2b)。纺锤结结构基于静电纺丝中常见的串珠现象制备:当射流进入远场区域,表面电荷间的静电斥力易引发不稳定性,低压下这种不稳定性会触发瑞利破裂,形成串珠状纳米网。
SDSN 集成润湿性、孔径、纤维结构三重 Janus 设计,其中纺锤结结构对传输动力学起主导作用。从疏水侧施加 5 μL 液滴时,SDSN 可在0.8 s 内完成吸收与跨层传输,单向传输速率约 6.25 μL s⁻¹(图 2c);而无纺锤结的对照纳米网需 13 s。在真实出汗场景中,液体从疏水侧初始渗入虽会受表面斥力与重力阻碍,但可快速接触亲水层;接触后毛细力占主导,主动将液体向上抽吸、对抗重力(图 2d)。实验验证:从疏水侧滴加 5 μL 液滴,带纺锤结的 SF12(13 kV)横向铺展速率比无纺锤结(19 kV)快 60%(135.95 mm² s⁻¹ vs 83.11 mm² s⁻¹,图2f);抗重力毛细上升速度快 180%(0.29 mm s⁻¹ vs 0.076 mm s⁻¹,图2g)。
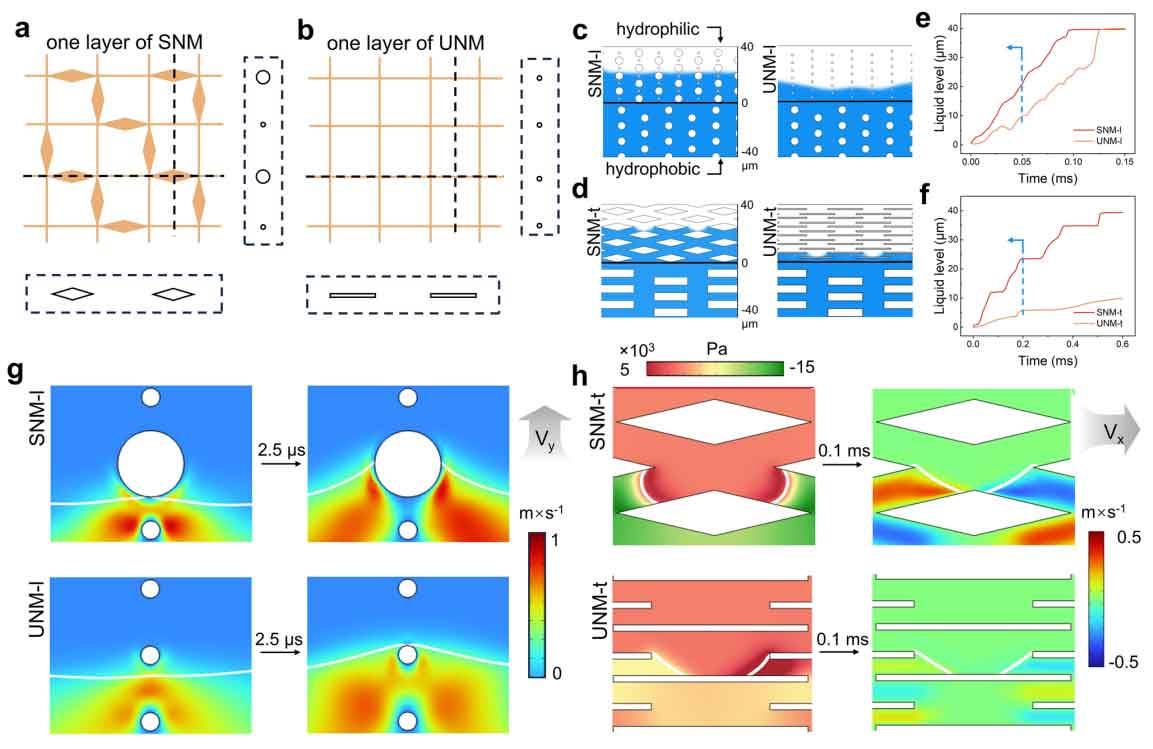
图3双架构双视角比较模型分析。
双结构、双视角对比模型框架
由于液体在纳米网内部的浸润与流动动力学难以通过仪器直接观测,本研究搭建了双结构、双视角对比模型框架,用于分析纳米网尺度下的液体驱动机理。
为进行对照,研究构建了两种模型:
均匀纳米网模型(UNM):顶层为无纺锤结的均匀纳米网
纺锤结构纳米网模型(SNM):引入可增强吸水能力的纺锤结构
将静电纺纳米网膜模拟为多层纤维结构,每层纤维正交排布,纤维直径与间距均取自 SEM 图像统计结果,得到两种模型的俯视图(SNM 见图 3a,UNM 见图 3b)。
研究分别考察纵向截面与横向截面(纵向视角:SNM-l、UNM-l;横向视角:SNM-t、UNM-t)。纵向截面显示,模型呈现由规则圆形结构组成的横截面构型(图 3c);横向视角下,纺锤结简化为菱形,均匀纤维简化为矩形(图 3d)。
当液体从下边界向上浸润时,SNM 在两种视角下均优于 UNM:
纵向视角流速提升约1.3 倍
横向视角流速提升约4 倍
与前述毛细爬升实验中 1.8 倍的提升结果一致(图 3e、f)。
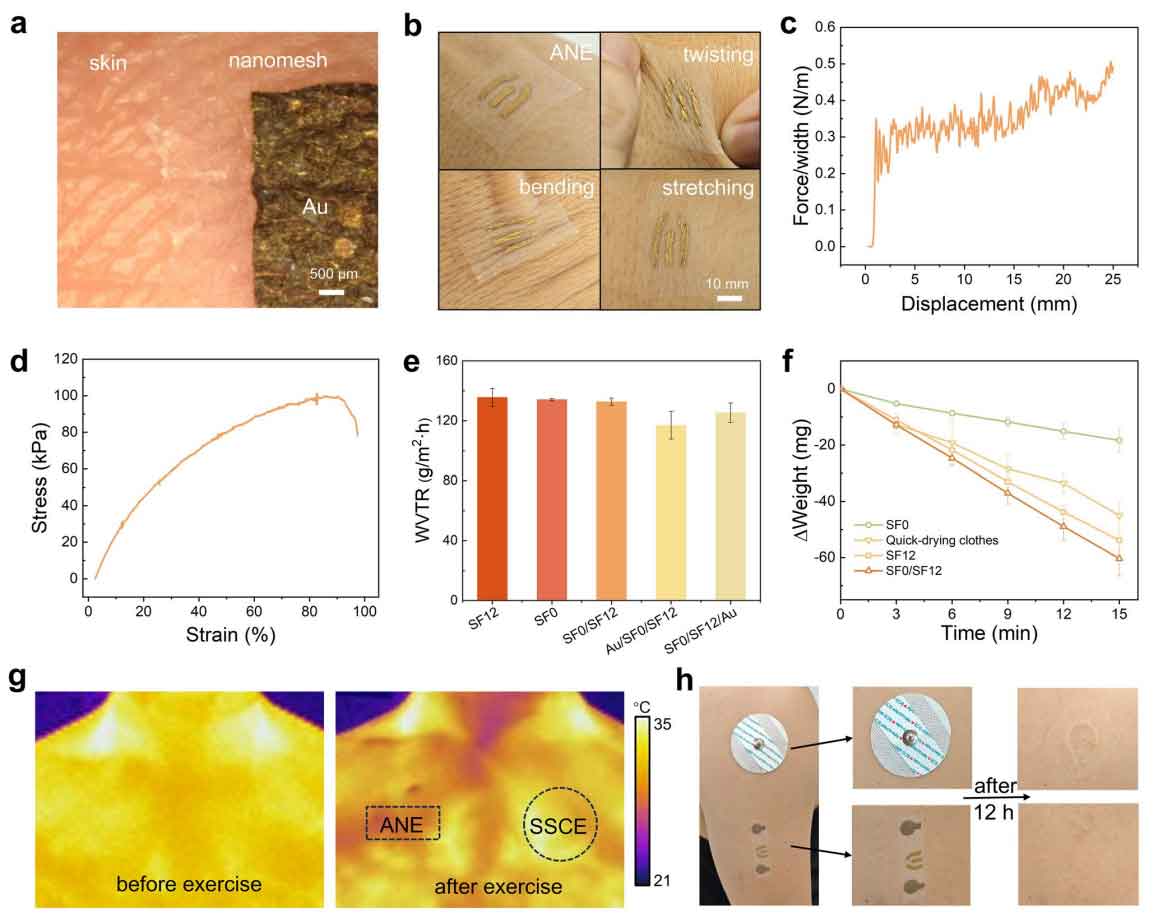
图4 ANE的表征。
金纳米网电极(ANE)的力学与生物相容性性能
汗液中的氢键与毛细作用确保电极与皮肤紧密贴合(图 4a)。无出汗状态时,用水润湿即可贴附皮肤;水分蒸发后,依靠超薄厚度带来的优异贴合性,通过范德华力维持黏附。ANE 在扭曲、弯曲、拉伸等各种形变下均能稳定贴附皮肤(图 4b)。剥离力测试可定量表征这一特性:10 mm 宽样品的剥离力约 3×10⁻³ N,远超皮肤最大形变时的弹性力 10 倍以上。因此电极可耐受肢体运动与皮肤拉伸,不发生界面分离或位移,有效抵御运动伪影(图 4c)。
湿润状态的电极可稳定附着于皮肤,这一稳定性也源于纳米网的高拉伸性,可拉伸至接近原长的两倍(图 4d)。水蒸气透过率测试表明(图 4e),SDSN 具备较高透气性能;且定向导汗设计未降低其透过性,WVTR 达 132.6 g m⁻² h⁻¹,与纯亲水/疏水层接近。SDSN 的液体蒸发速率显著优于单层纳米网与速干衣物(图 4f)。得益于高效汗液传输与蒸发能力,ANE 在运动中的热舒适性显著优于商用凝胶 Ag/AgCl 电极(SSCE)。
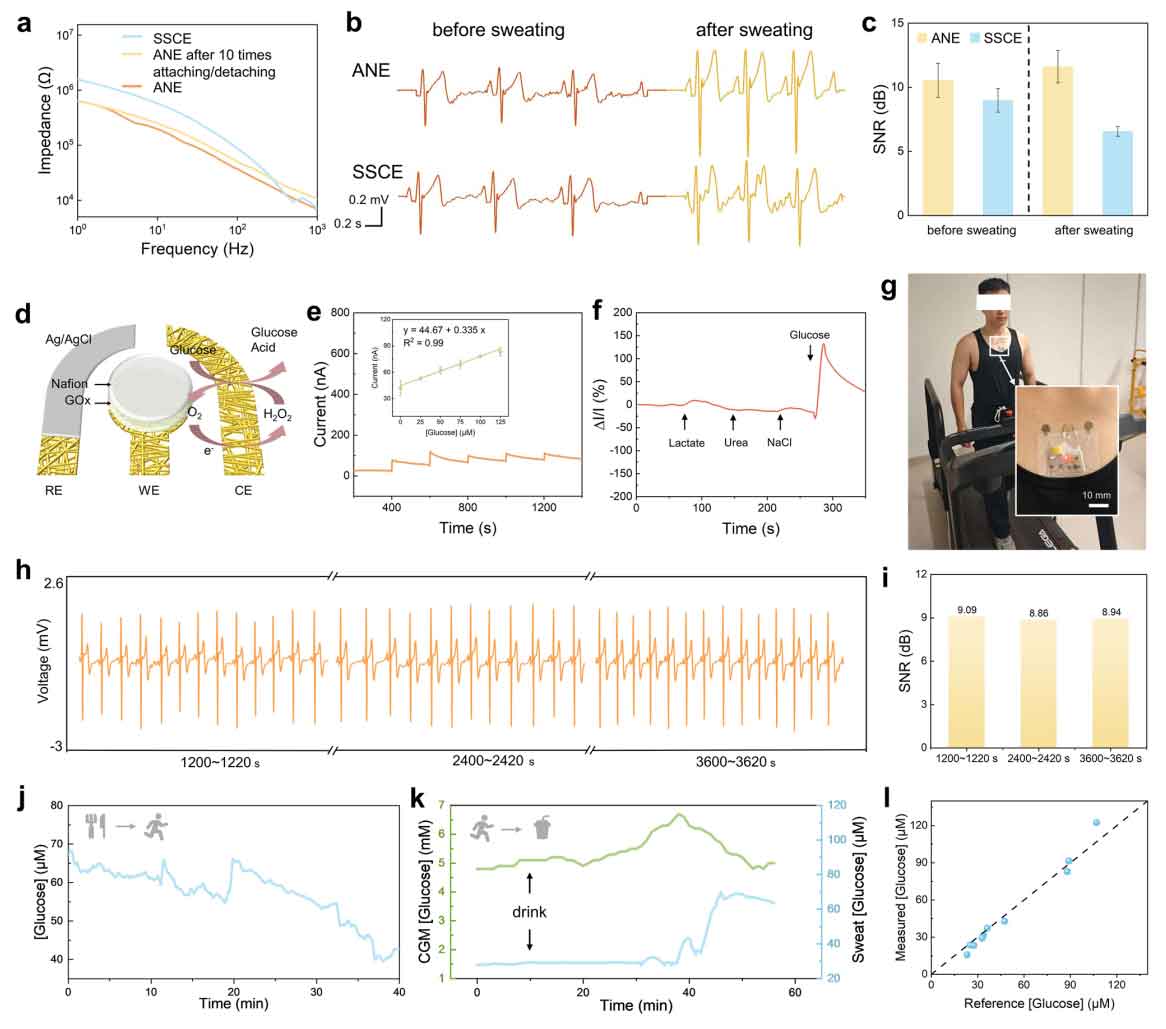
图5心电图与汗液血糖监测的应用。
系统在心电与汗液葡萄糖监测中的应用
ANE 与皮肤的界面阻抗低于 SSCE(1 Hz 时分别为 0.63 MΩ 和 1.57 MΩ),且在反复粘贴 — 剥离 10 次后仍能保持低阻抗(1 Hz 时 0.64 MΩ,图 5a),说明结构稳定且可重复使用。在出汗状态下,ANE 仍能保持清晰的心电波形,且运动后信号幅度有所提升,P 波、QRS 波群、T 波均可清晰分辨;与之对比,SSCE 出现基线漂移且信号幅度更低(图 5b)。
相应地,运动后 ANE 的信噪比从 10.5 dB 提升至 11.6 dB,而 SSCE 从 9.0 dB 降至 6.6 dB(图 5c)。这说明透气贴合的 ANE 可避免汗液液膜形成、降低界面噪声,而传统凝胶电极不透气、易被汗液干扰。总体而言,ANE 在温湿度与运动应力下能提供更稳定、更高质量的信号。
ANE 可实现酶介导的汗液葡萄糖检测,并具备稳定的电化学行为(图 5d)。电流法标定显示,电流随葡萄糖浓度阶梯式上升,灵敏度达到 335 nA mM⁻¹(图 5e)。传感器对汗液中常见干扰物(乳酸、尿素、氯化钠)具有良好抗干扰性(图 5f)。研究将电生理信号检测与生化传感结合柔性电子,构建了柔软、无线、多模态的表皮监测系统,实现整机透气与定向汗液管理(图 5g)。
心电数据可准确反映生理状态,如体力消耗增加时心率上升、信号幅度增强(图 5h)。运动 20、40、60 分钟时心电信号质量保持一致,信噪比维持在基线的 90% 以上(图 5i)。测试在餐后进行,观察到运动过程中汗液葡萄糖水平下降,反映餐后葡萄糖被消耗(图 5j)。汗液葡萄糖可实时反映能量消耗与代谢变化:受试者中途摄入高糖饮料后,葡萄糖水平明显上升,反映运动中糖摄入与消耗的动态过程(图 5k)。
原文链接:https://doi.org/10.1007/s40820-026-02115-w
