慢性伤口因免疫微环境失调与异常纤维化导致愈合障碍,造成严重的临床负担。伤口愈合涉及炎症、增殖与重塑的精密调控,其中巨噬细胞从促炎(M1)向抗炎(M2)表型的适时极化是炎症消退和组织再生的核心,而成纤维细胞过度活化为肌成纤维细胞并导致胶原异常沉积,则是瘢痕形成的主要病理机制。皮肤筋膜层作为修复细胞的源头与迁移支架,在引导有序再生中起核心作用,其作用机制为新型敷料设计提供了关键仿生靶点。因此,模拟筋膜的多级次纤维网络结构并实现免疫调节与纤维化抑制的时空调控,是推进慢性伤口修复的迫切需求。

近日,燕山大学张强团队在期刊《Advanced Functional Materials》上,发表了最新研究成果“Bioinspired Hydrogel Prepared by Core-Shell Nanofibers: Accelerating Wound Healing via Macrophage Polarization Modulation”。研究者通过模拟皮肤筋膜的多级次微纳复合结构,制备了具有光响应特性的载药核壳纳米纤维水凝胶(CA-DAF-BSA@PFD),实现时空次序调控,促进伤口修复过程。
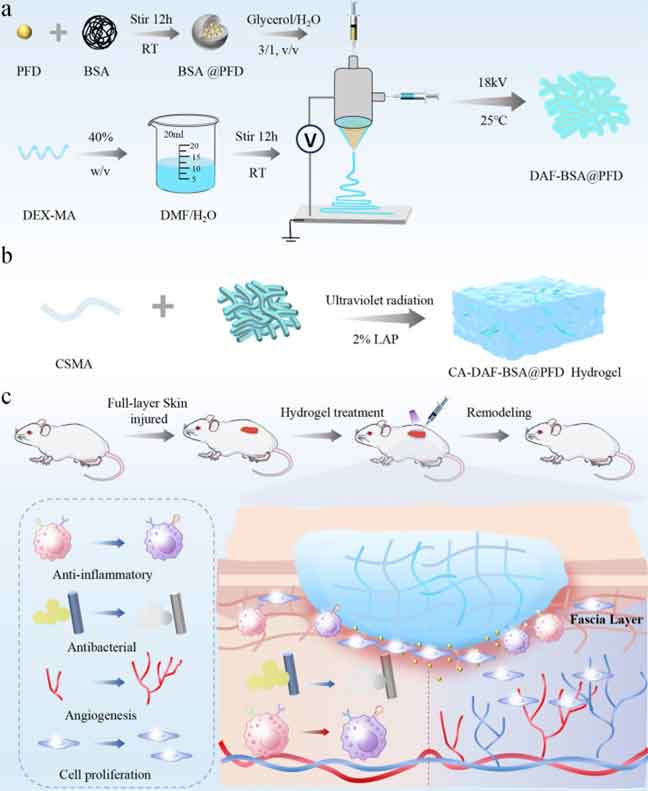
图1:仿筋膜核壳纳米纤维水凝胶示意图。
为模拟皮肤筋膜层的纤维网络结构,采用同轴静电纺丝技术制备了包载BSA@PFD纳米颗粒的甲基丙烯酰化葡聚糖纳米纤维(DAF-BSA@PFD)。其中,以甲基丙烯酰化葡聚糖(Dex-MA)为壳层,BSA@PFD纳米颗粒为芯层,成功构建出具有明显核壳结构的纳米纤维。扫描电镜结果显示,所制备的纳米纤维表面光滑,直径分布均匀,平均直径为602±31 nm(图2g)。透射电镜图像进一步证实其核壳形貌,壳层厚度约为39 nm,并可清晰观察到均匀分布于纤维内部的纳米颗粒(图2j)。荧光成像结果同样支持纳米颗粒在纤维芯层的有效负载。
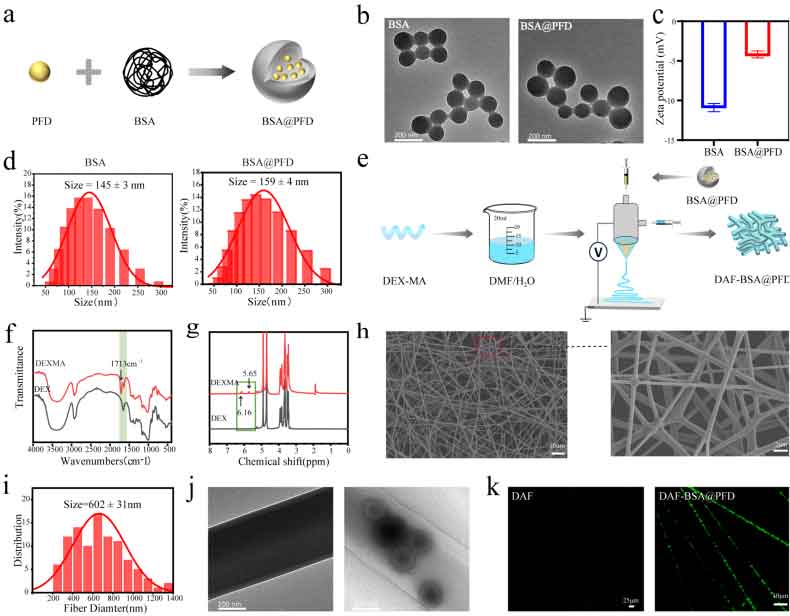
图2:载药核壳纤维的制备与表征。
为实现对皮肤间质多级次结构的仿生模拟,将DAF-BSA@PFD纳米纤维与甲基丙烯酰化硫酸软骨素(CA)水凝胶复合,构建出具有微米级多孔结构与纳米级纤维网络的双尺度仿生材料(CA-DAF-BSA@PFD)。通过与皮肤筋膜层对比,确定30%含量的纳米纤维作为仿生模拟最佳选择(图3),能够有效改善水凝胶的力学性能,同时保持适宜的机械强度和韧性,为后续生物学应用奠定了基础。
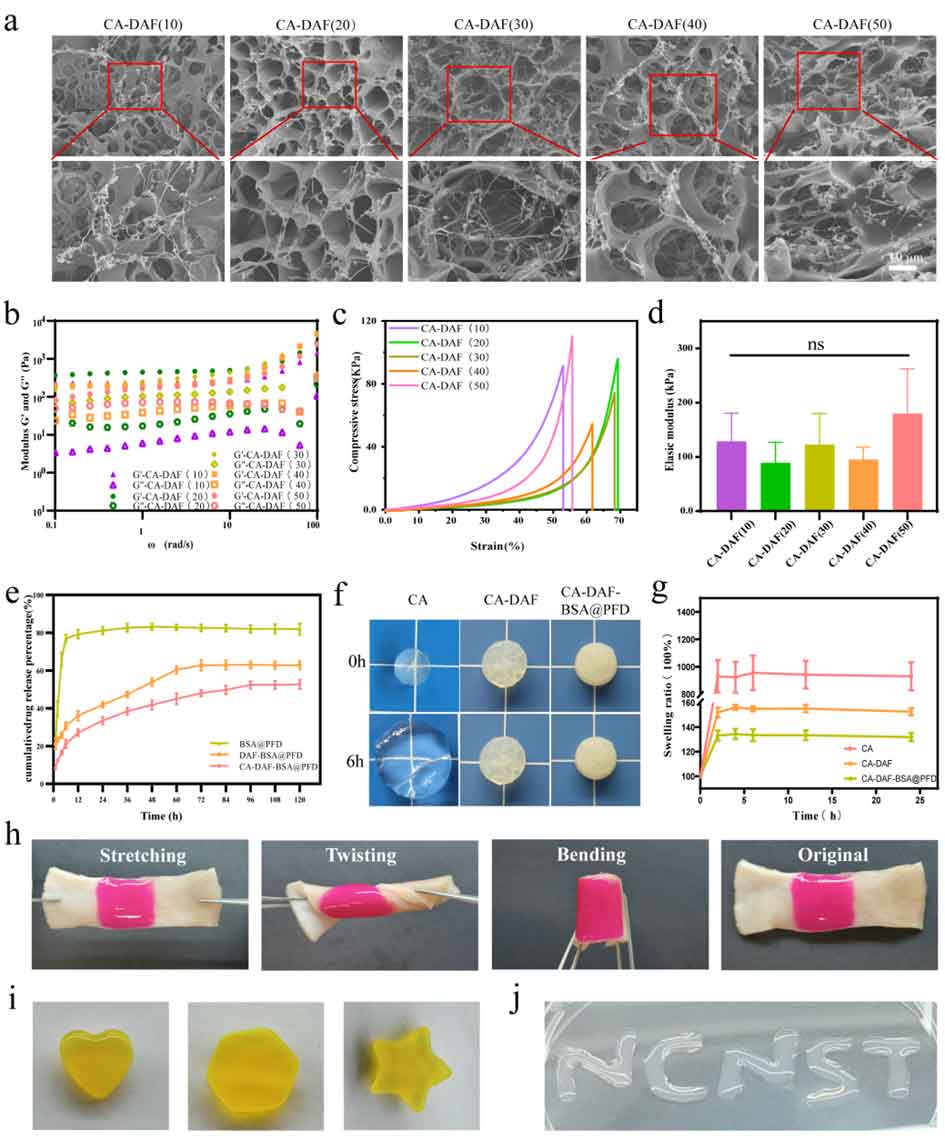
图3:CA-DAF-BSA@PFD水凝胶的制备与表征。
该水凝胶展现出良好的黏弹性、可注射性、抗溶胀性、抗菌性、生物安全性,为创面修复提供了理想的微环境支撑。体外实验证实,CA-DAF-BSA@PFD水凝胶可显著促进巨噬细胞向M2型极化(图4),同时抑制成纤维细胞向肌成纤维细胞分化,表明其具有调控炎症微环境和抑制瘢痕形成的双重功能。
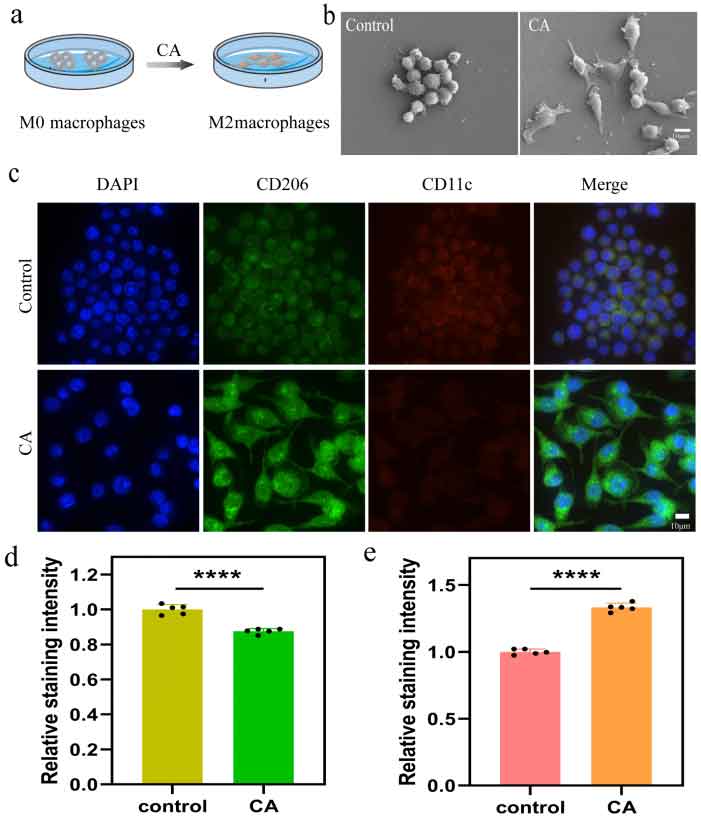
图4:水凝胶对巨噬细胞极化的调控作用。
在动物全层皮肤缺损模型中,CA-DAF-BSA@PFD水凝胶能显著促进肉芽组织生长与再上皮化,并抑制胶原过度沉积与排列紊乱,从而有效减少瘢痕形成。其修复机制呈现明显的时空序贯特性:前期通过水凝胶基质调控免疫微环境,诱导巨噬细胞向M2表型转换,上调抗炎因子IL-10并下调促炎因子IL-6的表达,加速炎症消退;后期借助纳米纤维缓释PFD,持续抑制肌成纤维细胞活化与异常细胞外基质累积。此外,该水凝胶还可促进伤口血管新生,为组织再生提供营养支持。
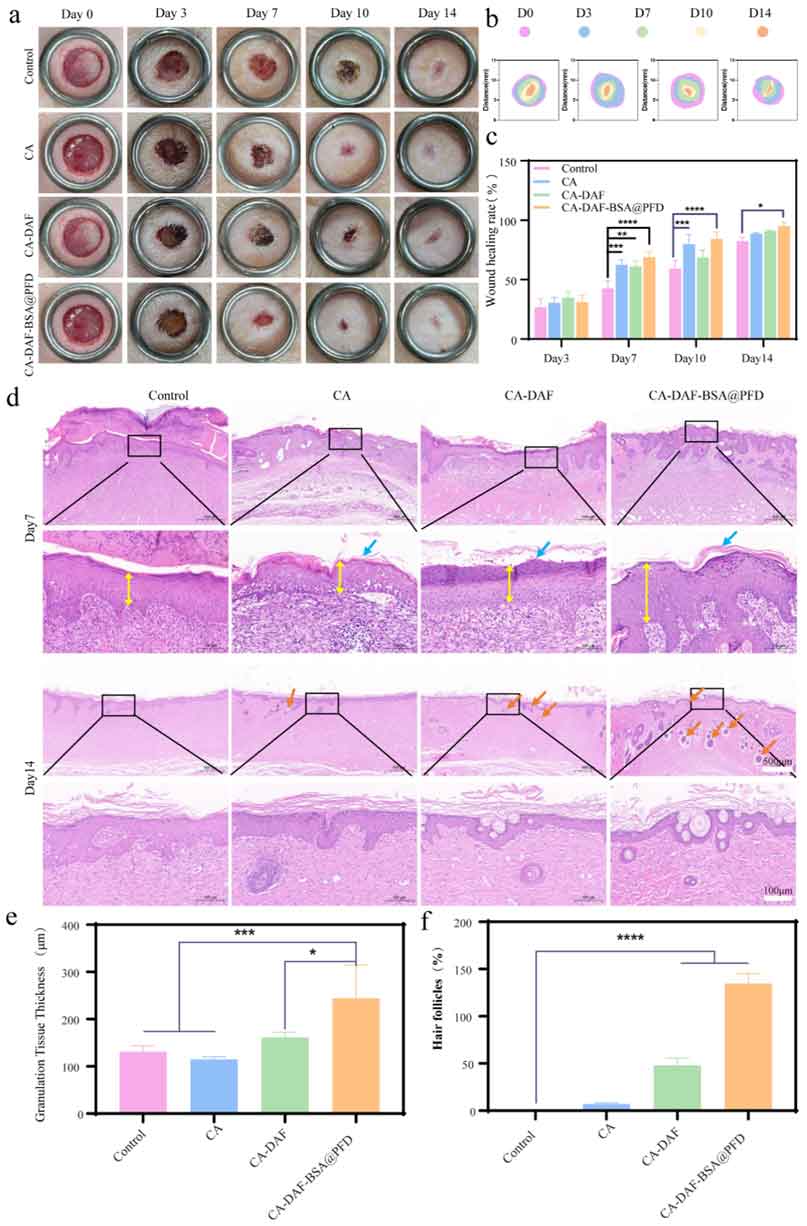
图5:伤口修复评估
综上所述,该研究通过仿生筋膜结构设计,构建了一种具备时空序贯调控功能的纳米纤维复合水凝胶,为促进慢性伤口愈合、抑制瘢痕形成提供了一种具有转化潜力的新材料策略。
论文链接: https://doi.org/10.1002/adfm.202524234
