组织器官的形成、稳态维持及损伤修复过程,本质上是一个由多尺度、多维度因素协同调控的复杂过程。而生物电信号在其中扮演着至关重要的角色,如调控细胞的增殖、分化、迁移等关键生命活动,以及组织微环境的重建。然而,传统的组织工程支架往往难以有效地模拟体内动态变化的电微环境,缺乏主动、精准调控细胞行为的手段。在此背景下,压电电纺纤维因其高度柔性、仿生细胞外基质结构、形貌可调性以及将机械刺激转化为电信号的能力,在组织工程和生物医学领域展现出巨大的潜力。但如何优化电纺纤维的压电性能进一步调控组织修复仍是一项重大挑战。

基于此,清华大学李舟教授团队在期刊《Science Bulletin》上,发表了最新综述“Piezoelectric electrospun fibers for tissue regeneration: synergizing microarchitecture and enhancement strategies”。该文章创新性地全面综述了压电电纺纤维及目前多维度增强压电性的策略,重点阐述了纤维微结构设计及填料增强压电性能的策略。同时介绍了电纺纤维产生电信号的刺激方式,并展示了在组织工程领域的多元应用。此外,本综述还探讨了压电电纺纤维面临的挑战与未来发展方向,旨在为设计新型高性能压电支架及下一代组织支架提供重要指导。
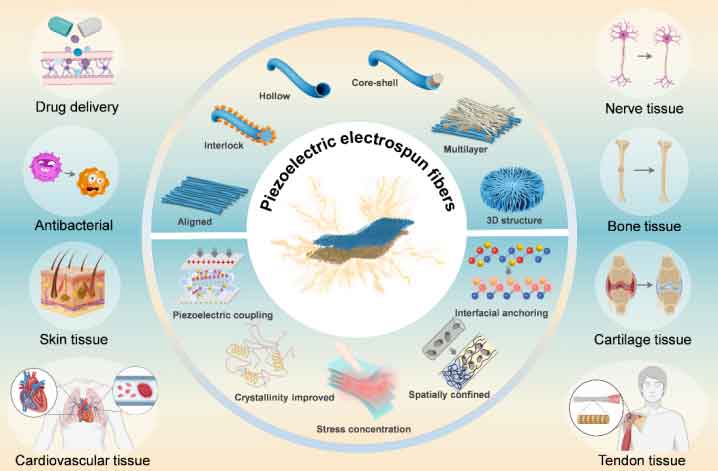
图1: 压电纤维微结构设计/增强策略及其在组织工程中的应用
该综述概述了各种压电电纺纤维的种类,介绍从纺丝过程的调控方法以及传统压电性能的增强策略(退火和极化等)。重点介绍目前电纺纤维微结构(取向、互锁、核壳、空心、多层和三维结构)的自增强策略,创新地总结了现有填料与压电纤维复合体系提升压电性能的方法,包括压电耦合、结晶度改善、纤维内应力集中、空间限制效应和界面效应锚定增强策略。此外,还介绍了压电纤维上产生电信号的不同方法,并展示其在多种生物医学应用,如药物递送、抗菌和创面愈合、神经组织工程、心血管组织工程、骨组织工程、软骨组织工程及其他组织等。
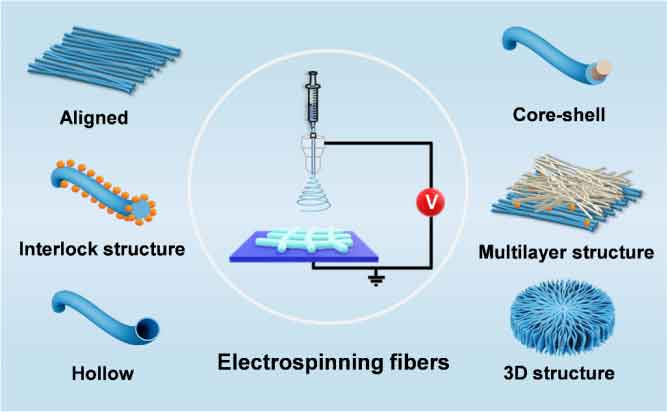
图2: 压电纤维支架不同微结构的设计策略
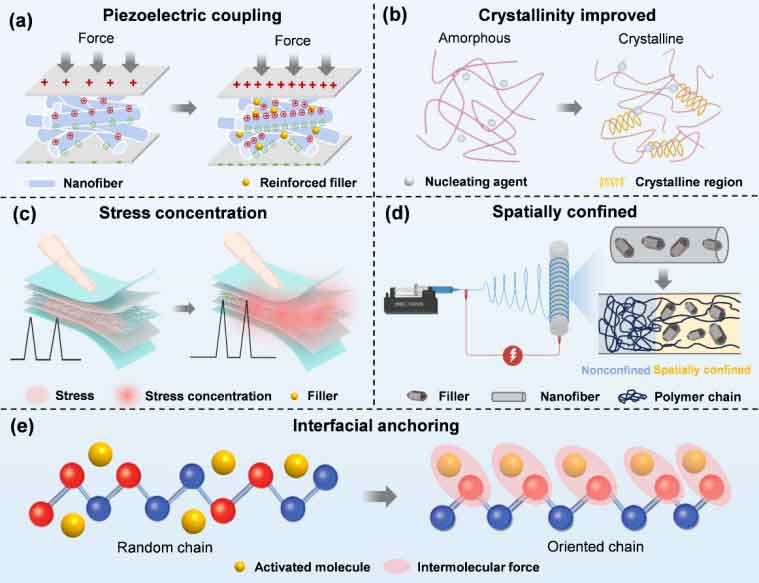
图3: 电纺纤维压电性能的增强策略:(a)压电耦合, (b)结晶度改善;(c)应力集中效应,(d)空间限制效应,(e)界面锚定策略
最后文章从如何优化电纺纤维压电性能、探究细胞与组织相互作用机制及推动临床转化三个角度,深入探讨了压电电纺纤维面临的挑战与未来发展方向。
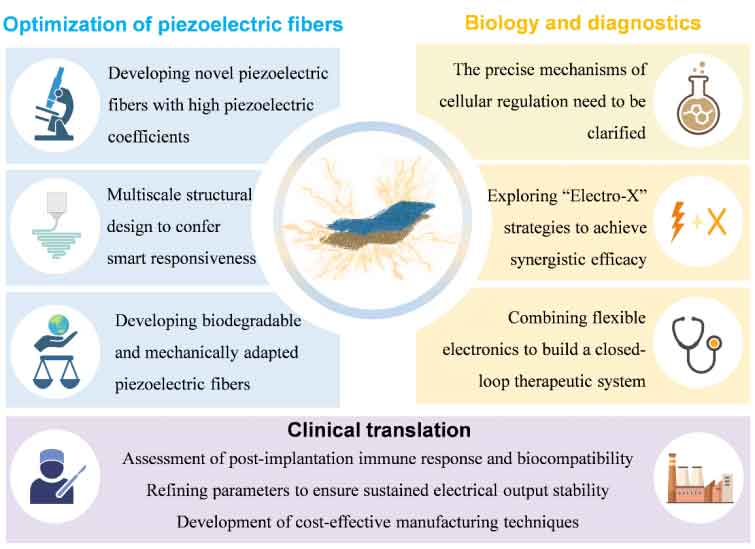
图4: 压电纤维在组织再生中的关键问题和未来发展方向
论文链接:https://doi.org/10.1016/j.scib.2025.12.031
人物简介:
李舟,博士生导师。清华大学生物医学工程学院长聘副教授、清华大学临床医学院/北京清华长庚医院研究员、北京清华长庚医院健康科技研发中心主任。获国家杰青、北京市杰青、国家万人青拔、教育部新世纪、北京市青拔和北京市科技新星。在国际上率先提出人体自供能生物电子器件,获北京市科学技术二等奖,已在心脏起搏器上开展技术转化。主持国家自然科学基金、国家重点研发计划、新曦颠覆式技术创新基金、中科院先导专项、北京市重点项目、北京市自然科学基金-海淀原始创新基金重点项目和华为技术合作项目等多项基金课题。在Nature Biomedical Engineering, Nature Reviews Cardiology, Cell Biomaterials, Science Advances, Nature Communications等期刊上共发表论文300余篇,3 篇入选ESI前1‰热点论文和29篇入选ESI前1%高被引论文,论文数、H指数、被引次数等排名全球前1%,并入选科睿唯安2024年度“全球高被引科学家”名单。
