周围神经损伤是神经系统最常见的创伤之一,全球有数百万患者受其影响。神经导管为周围神经修复提供了一种有效策略,但其临床疗效仍有待进一步提高。血小板因能释放多种生物活性生长因子,在神经修复领域展现出广阔潜力;然而,其易于快速活化的特性往往导致生长因子爆释,限制了长效血小板治疗产品的研发。

近日,四川大学华西医院苟马玲教授团队在期刊《Bioactive Materials》上发表研究论文“Bioprinting of live platelet-loaded nerve conduit using energy-dissipative hydrogel”,张家梅、吴文碧、任亚为共同第一作者。研究者利用能量耗散型水凝胶提升血小板的存活时间及持续释放促组织再生因子的能力,结合快速生物3D打印技术,研制了一种载血小板的神经导管,有望为外周神经修复提供新的方法(图1)。
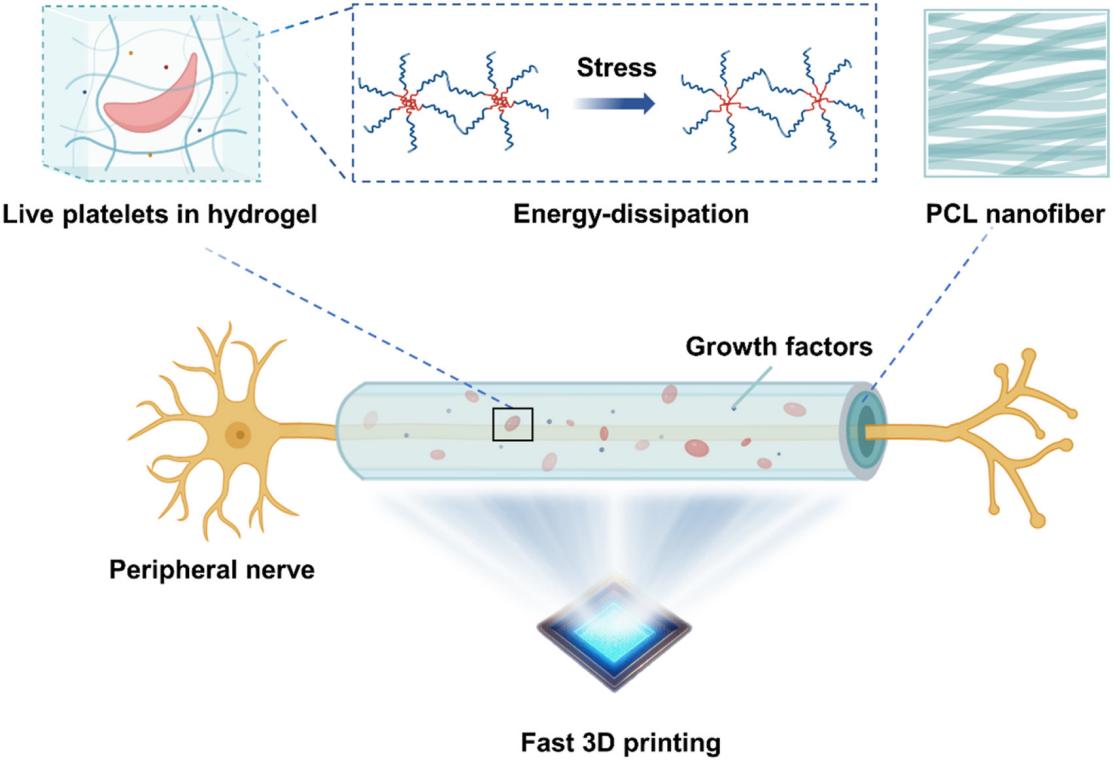
图1: 快速3D打印载血小板的神经导管,利用能量耗散型水凝胶改善血小板的体内存活及持续释放生长因子的能力。
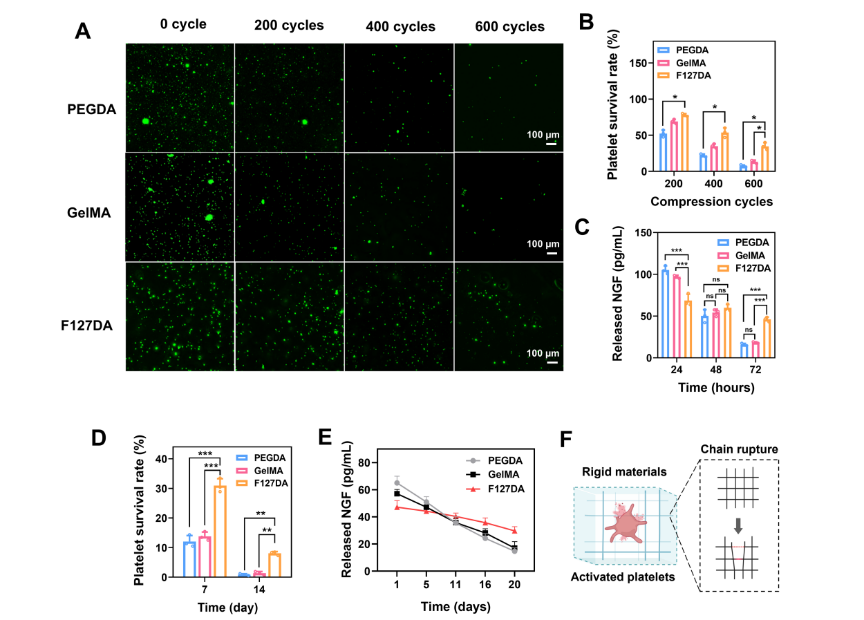
图2:能量耗散水凝胶通过减轻形变相关内应力对血小板的损伤以改善血小板的存活。
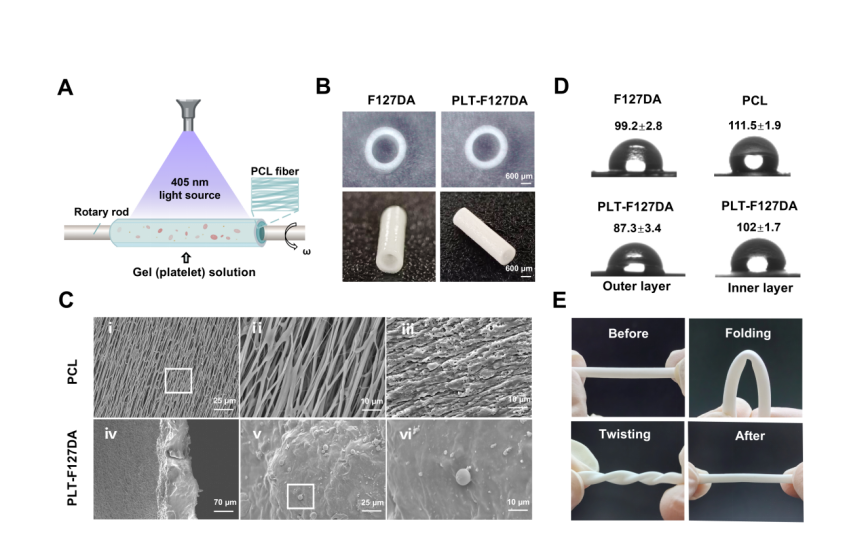
图3:新型快速3D打印技术用于将载血小板水凝胶与静电纺丝材料复合,以构建具有较好力学性能的神经导管。
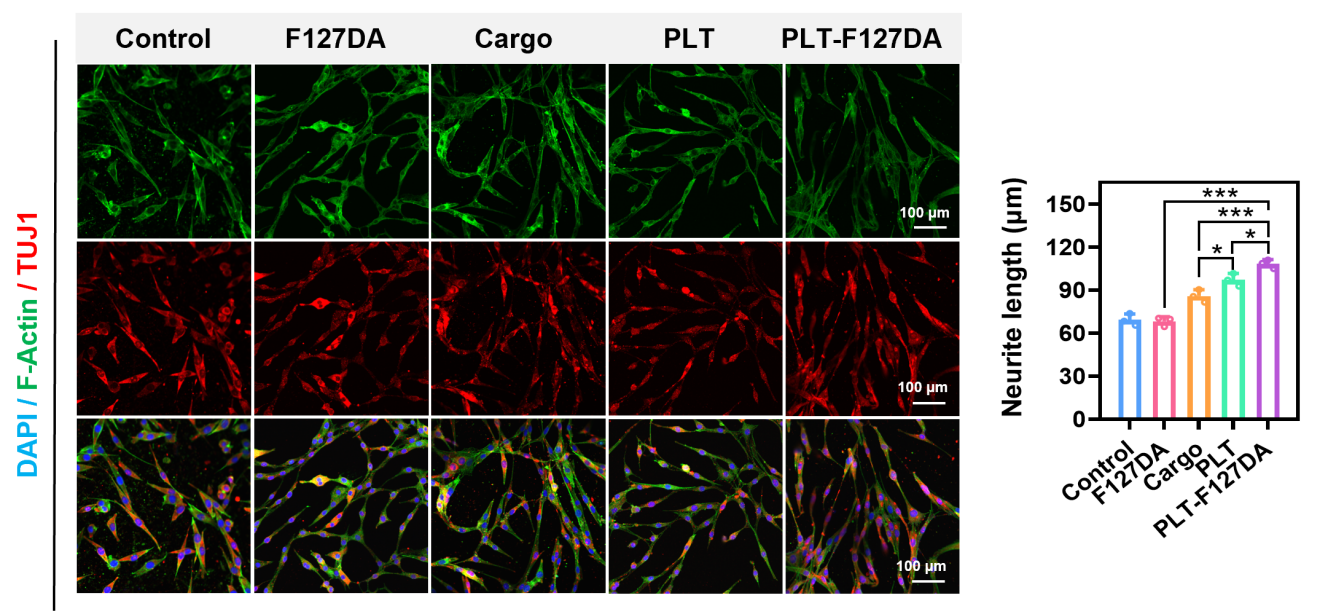
图4:载血小板神经导管通过释放生长因子增强神经细胞的功能。
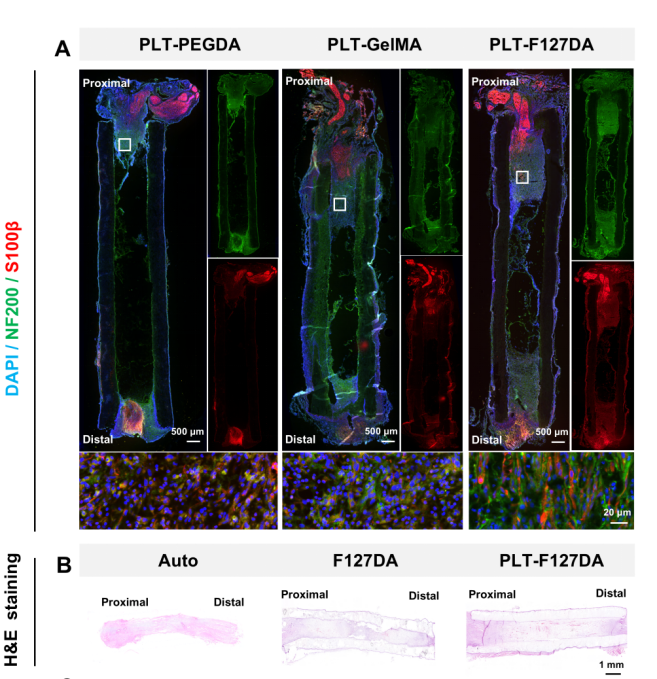
图5:载血小板神经导管载体内有效促进外周神经修复。
本研究展示了一种新型的长效缓释生长因子的载血小板神经导管。该导管采用定制式3D打印技术将负载血小板的能量耗散水凝胶快速涂覆在静电纺丝导管上。这种水凝胶通过其内部的纳米胶束耗散能量,能在形变过程中减轻血小板受应力诱导的激活,在经历600次循环压缩后,血小板存活率仍可达34.7%。血小板在该水凝胶中可存活超过两周,从而实现神经生长因子(NGF)和血管内皮生长因子(VEGF)等生长因子持续释放20天以上。此外,该导管还具有良好的机械性能,包括抗压缩和抗拉伸能力,足以支持手术缝合和在体内的结构稳定性。植入12周后,该导管通过提供富含生长因子的微环境,有效促进了神经修复并取得了良好的功能恢复效果,展现了潜在的临床应用前景。
论文链接:https://doi.org/10.1016/j.bioactmat.2025.11.021
