干细胞治疗已成为慢性创面管理的一种有前景的策略。然而,在糖尿病创面愈合中,由于受到持续缺氧、过量活性氧(ROS)和持久炎性微环境等因素的不良影响导致其疗效有限。开发能够适应这些不良微环境的修复材料,有望增强干细胞的存活与功能,从而改善治疗效果。

2025年9月10日,上海大学刘媛媛、上海交通大学医学院附属新华医院苏佳灿、马玉海和海军军医大学第一附属医院肖仕初在期刊《Advanced Fiber Materials》上在线发表题为“In‑Situ Fabricated Living Nanofiber Scaffolds with Stem Cell‑Chlorella pyrenoidosa for Synergy Enhance Diabetic Wound Healing”的研究论文,该研究针对糖尿病创面中干细胞存活与功能受限的瓶颈问题,创新性提出一种干细胞与功能化纳米纤维支架的协同治疗体系。
首先,通过原位双组分交替静电纺丝技术构建聚环氧乙烷/聚乙烯醇缩丁醛(PEO/PVB)三维梯度结构纳米纤维支架,结合原位细胞电纺技术实现脐带间充质干细胞(UC-MSCs)的高密度、高活性均匀负载,形成“活体纳米纤维支架(LNFS)”。进一步整合蛋白核小球藻(CP)赋予支架持续供氧与活性氧清除功能,协同优化创面微环境。体内实验表明,LNFS@CP通过改善渗出液吸收、炎症抑制、胶原沉积及血管新生从而显著加速糖尿病创面愈合。
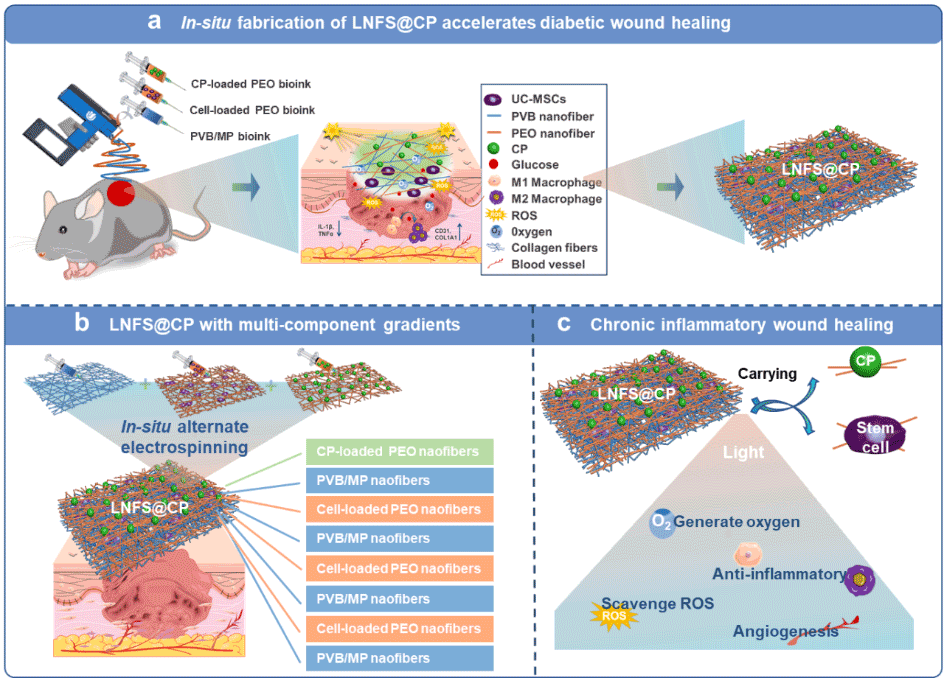
图1采用原位双组分交替静电纺丝技术制备LNFS@CP。
如图1a所示,使用便携式静电纺丝器械,通过交替静电纺丝技术实现LNFS@CP的原位构建,加速糖尿病创面愈合。利用双组分交替静电纺丝技术,成功制备了复合多组分梯度支架-LNFS@CP,该支架由含有贻贝粘附蛋白(MP)的纳米纤维、负载UC-MSC的PEO纳米纤维以及负载CP的PEO纳米纤维组成(图1b)。在体实验表明,原位制备的LNFS@CP显示出增强型协同治疗作用,包括产氧、清除ROS、抑制炎症以及促进血管生成,从而改善微环境并加速糖尿病创面愈合(图1c)。
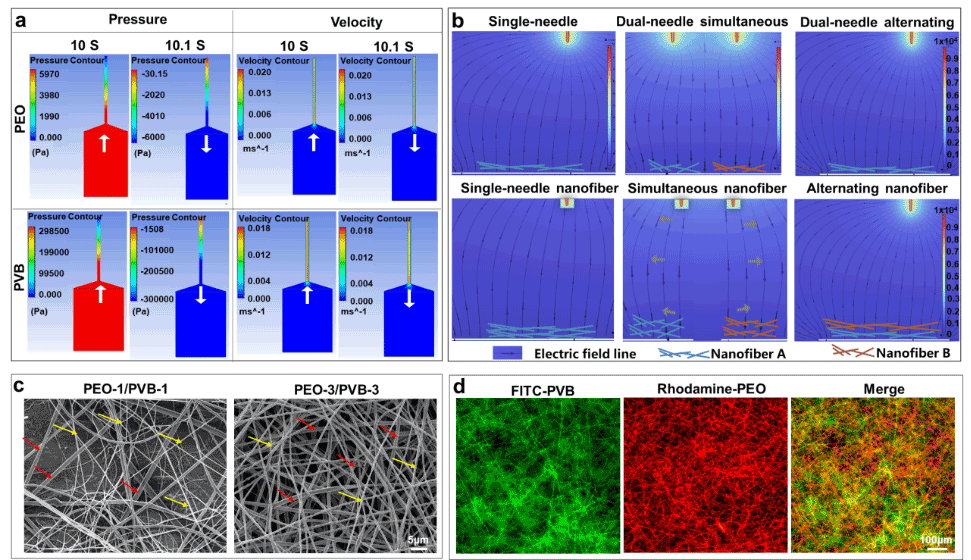
图2 原位交替静电纺丝技术构建双组分三维梯度结构支架,突破传统单组分纳米纤维支架的力学与生物学局限性。
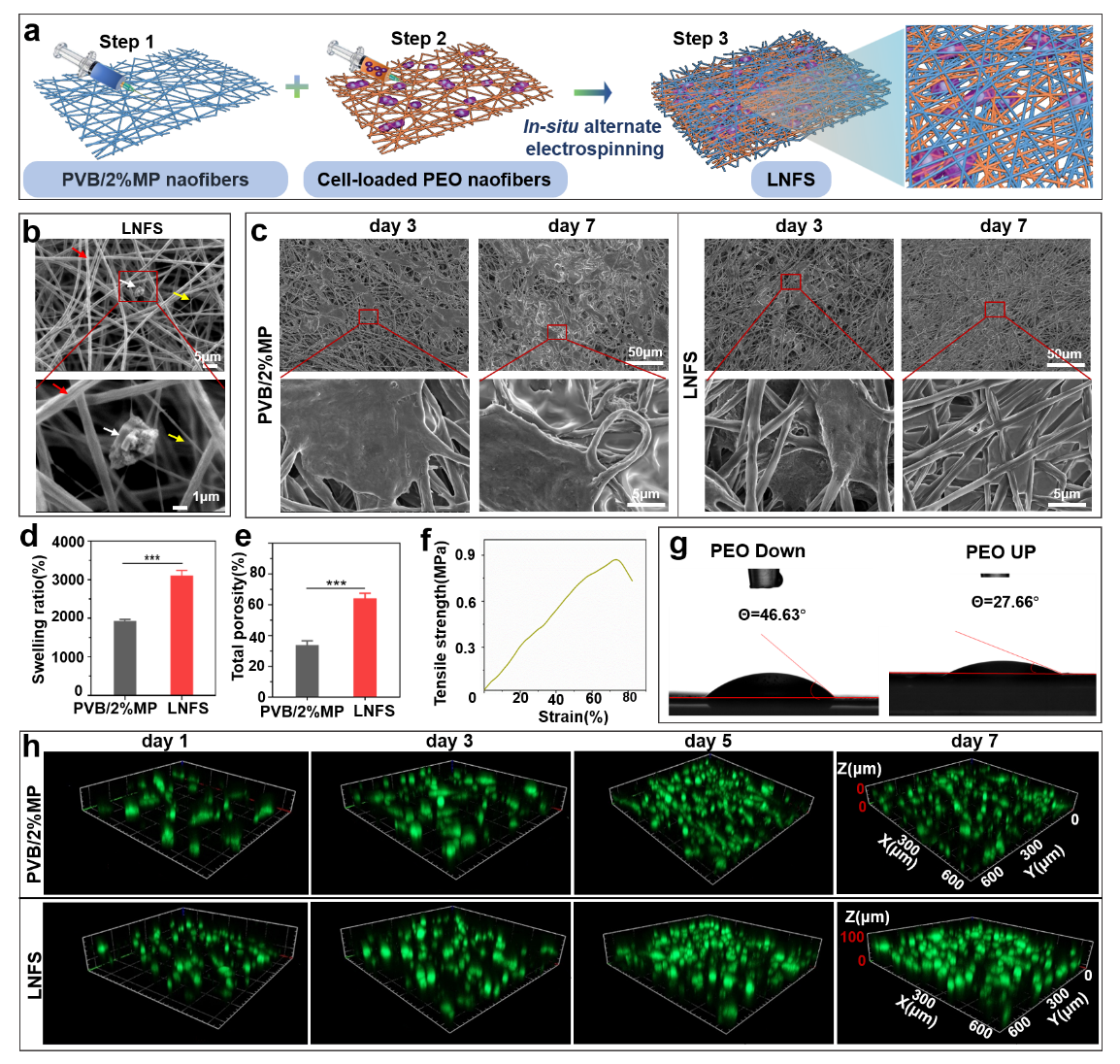
图3结合原位细胞电纺和交替静电纺丝技术,实现UC-MSCs在三维支架中的高密度、高活性均匀分布,克服传统接种法的细胞分布不均与低效问题。
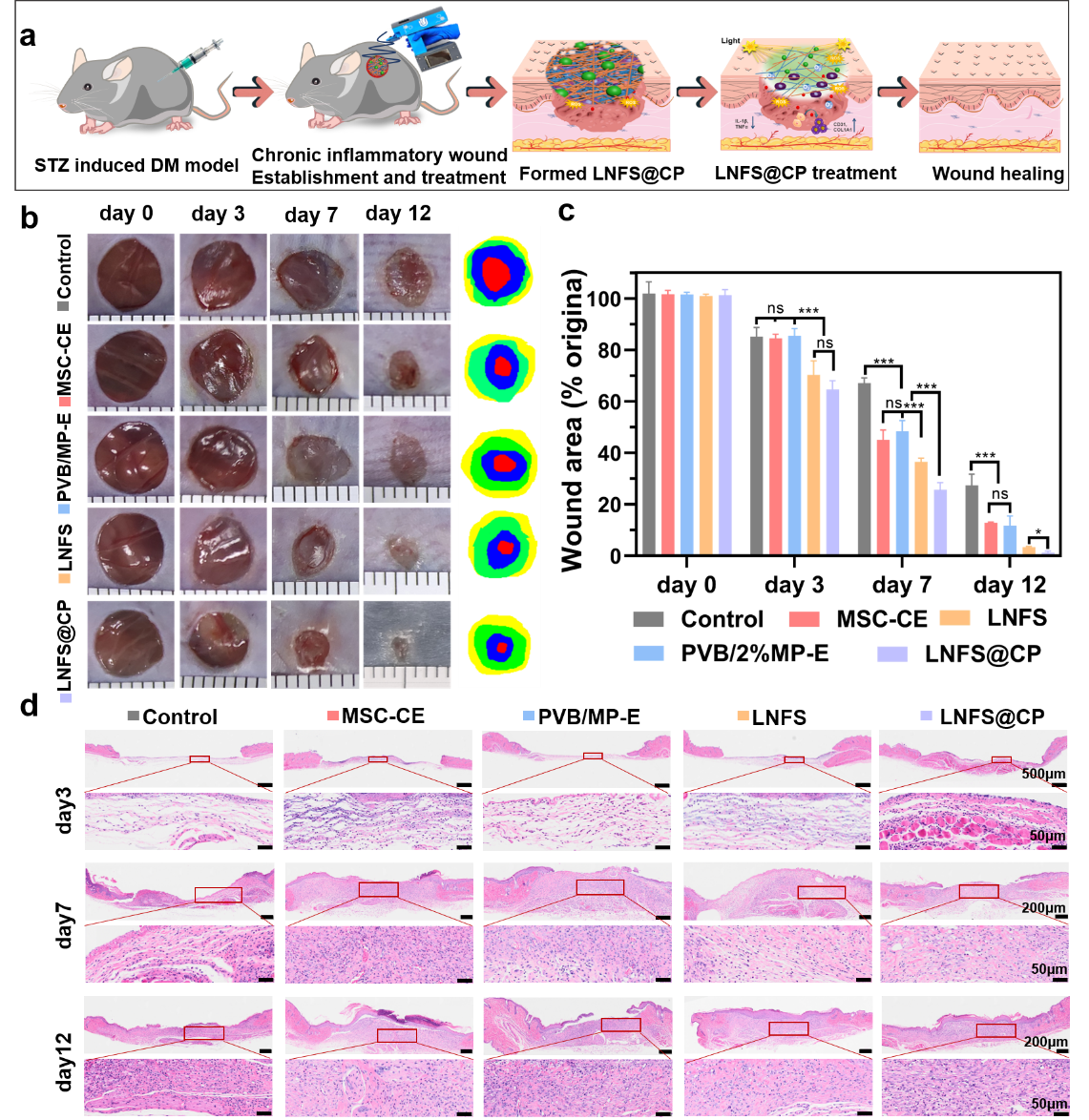
图4 CP提出“非接触式三维干细胞递送”策略,建立“微环境重塑-干细胞功能增强”双向协同治疗模式,为干细胞治疗提供了安全新颖的工程化递送平台。
结论
本研究首次提出“非接触式三维干细胞递送”策略,利用便携式静电纺丝器械原位构建了兼具微环境调控与干细胞功能增强的多功能生物支架LNFS@CP,为糖尿病创面治疗提供了创新解决方案。此外,该工作为复杂病理微环境下的组织再生提供了多维度协同干预的新思路,具有显著的临床转化潜力。
论文链接:https://link.springer.com/article/10.1007/s42765-025-00604-y
