
交通事故和自然灾害造成的急性创伤日益普遍,带来了多方面的挑战,如不规则伤口出血和易受微生物感染。中国科学院上海硅酸研究所刘宣勇、邱家军与上海市徐汇区口腔医院钱文昊合作,制备了与单宁酸基纳米铜(CTZP)配合的原位电纺丝玉米蛋白/聚乙烯吡咯烷酮纳米纤维生物活性敷料。CTZP在大鼠断尾模型中具有快速止血作用。体外凝血实验验证了CTZP能在1 min内实现凝血。研究发现,CTZP可通过PI3K-Akt信号通路通过TBXAS1的表达激活血小板。此外,体外成管实验表明,CTZP具有促进血管生成的作用。qPCR结果显示,玉米醇溶蛋白/聚乙烯吡咯烷酮(ZP)底物可以通过提高VEGF的生成来促进血管生成。此外,单宁酸铜纳米颗粒(Cu@TA)的加入进一步增强了VEGF的促进作用,并通过PI3K-Akt信号通路协同上调eNOS的表达,这与血小板活化的途径相同。此外,体内免疫化学结果证实了血管生成相关蛋白VEGF和CD31的上调。
另外,Cu@TA纳米粒子通过类芬顿反应生成羟基自由基和铜离子释放,使CTZP敷料具有较强的抗菌活性。最终,利用金黄色葡萄球菌感染的大鼠伤口模型进行体内实验,证实了CTZP具有显著的伤口愈合作用。 这些发现促进了原位静电纺丝技术在急性创伤护理中的实际应用,为设计止血、抗感染和血管生成伤口敷料提供了理论和材料上的见解。相关研究成果以“Point-of-care treatment of acute skin wound by portable in-situ electrospinning nanofiber dressings with rapid hemostasis, anti-infection, and angiogenesis effects”为题目,发表在期刊《Bioactive Materials》上。
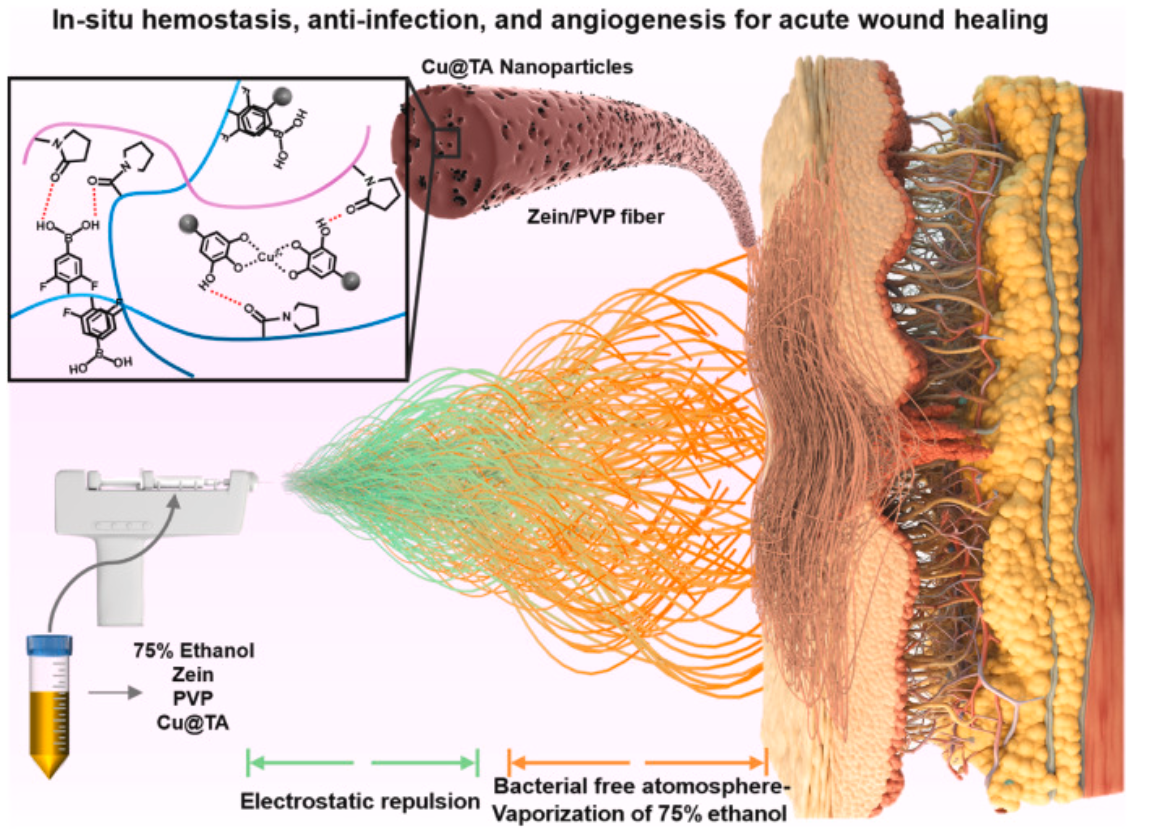
方案1 掺杂单宁酸基铜纳米粒子的原位静电纺丝玉米蛋白/PVP复合纳米纤维伤口敷料,通过止血、抗菌和血管生成作用增强伤口愈合。
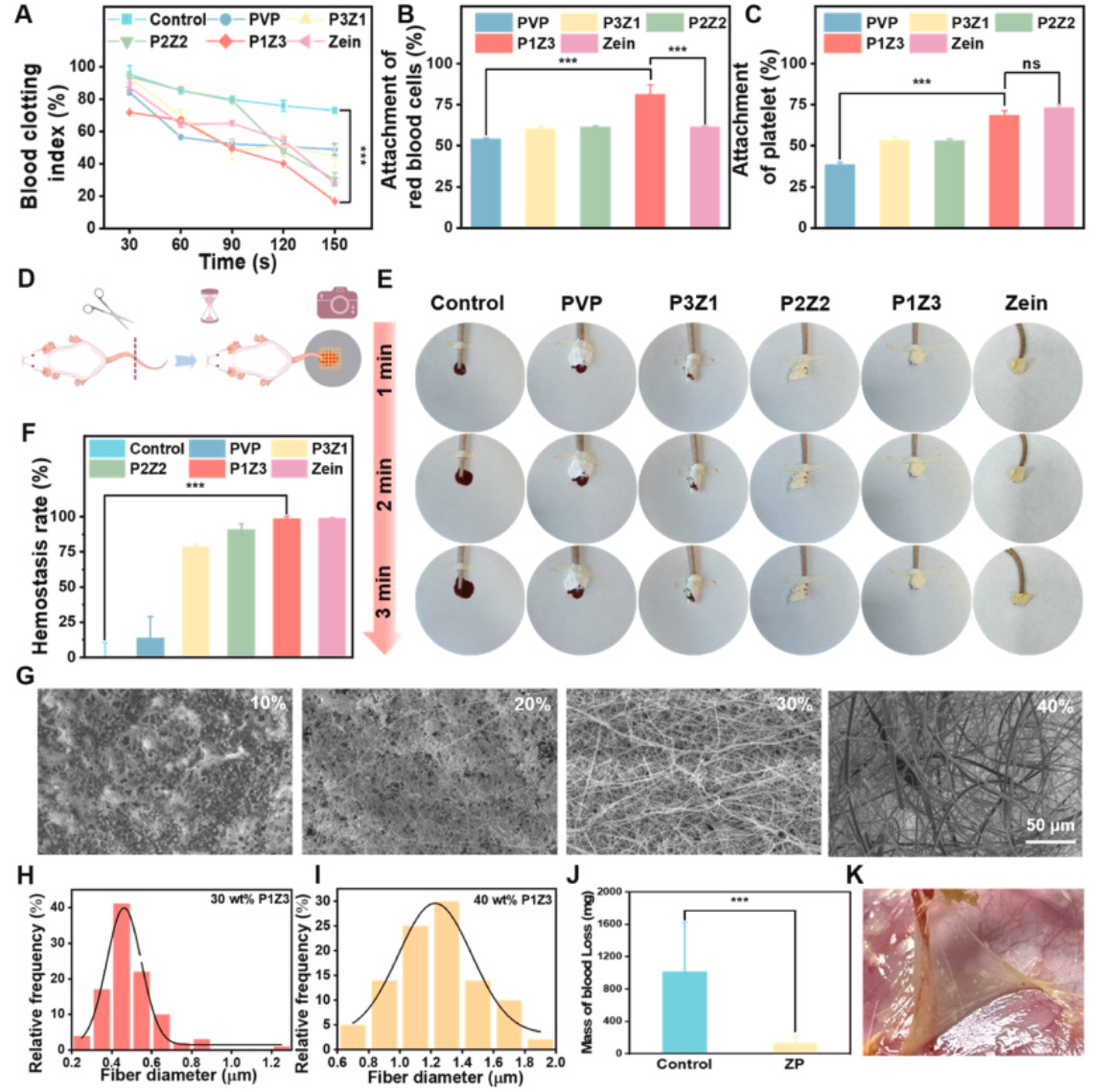
图1 筛选不同组分比的玉米蛋白/PVP纤维。通过体外凝血实验,包括凝血指数(A)、红细胞附着(B)和血小板附着(C),评估各种样品的止血性能。体内开放性出血大鼠断尾模型示意图(D)及不同组在3 min内对应的代表性照片(E)。各组3 min后止血率定量结果(F)。不同浓度P1Z3 (G)纤维膜的SEM形貌。P1Z3为30 wt% (H)和40 wt% (I)时纤维直径分布。重型肝损伤模型大鼠失血量定量记录(J)。大鼠皮下组织原位静电纺丝ZP纳米纤维膜图像(K)。
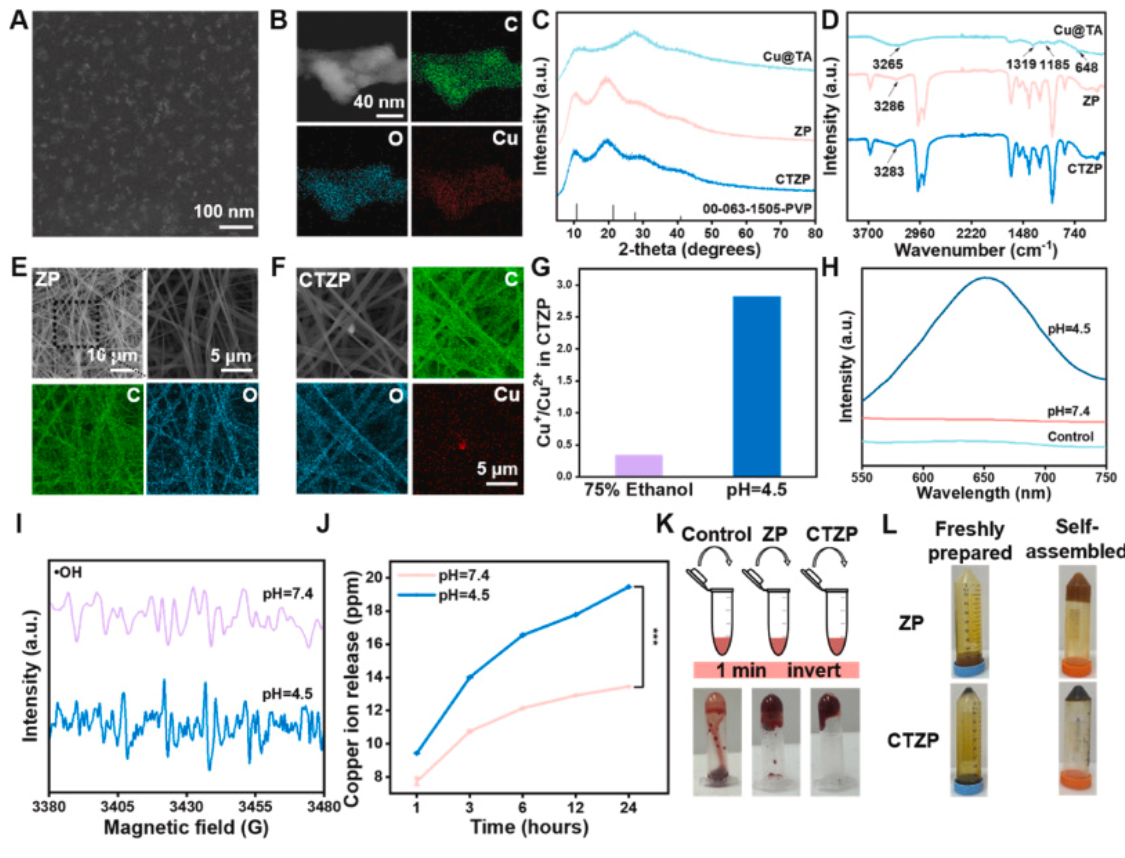
图2 Cu@TA NPs, ZP和CTZP的表征。HAADF-STEM中Cu@TA的形态(A)和对应的EDS高倍成像(B)。Cu@TA、ZP和CTZP的XRD谱图(C)和FTIR谱图(D). (E) ZP的SEM形貌和元素映射图。(F)CTZP的SEM形貌及相应的元素图谱。(G) Cu@TA分别在75%乙醇和pH=4.5的醋酸盐缓冲液中孵育后Cu+/Cu2+离子的比值。在pH=4.5与pH=7.4乙酸缓冲液中Cu@TA NPs在TMB测试中550-750 nm波长范围内的吸光度(H)和电子顺磁共振对不同pH下Cu@TA NPs的•OH检测(I)。(J)不同pH条件下CTZP的铜离子累计释放量(J)不同pH条件下CTZP累积释放的铜离子。(K) ZP和CTZP纳米纤维膜接触1min后大鼠全血倒置。(L)新鲜制备和自组装前体溶液的代表性光学照片。
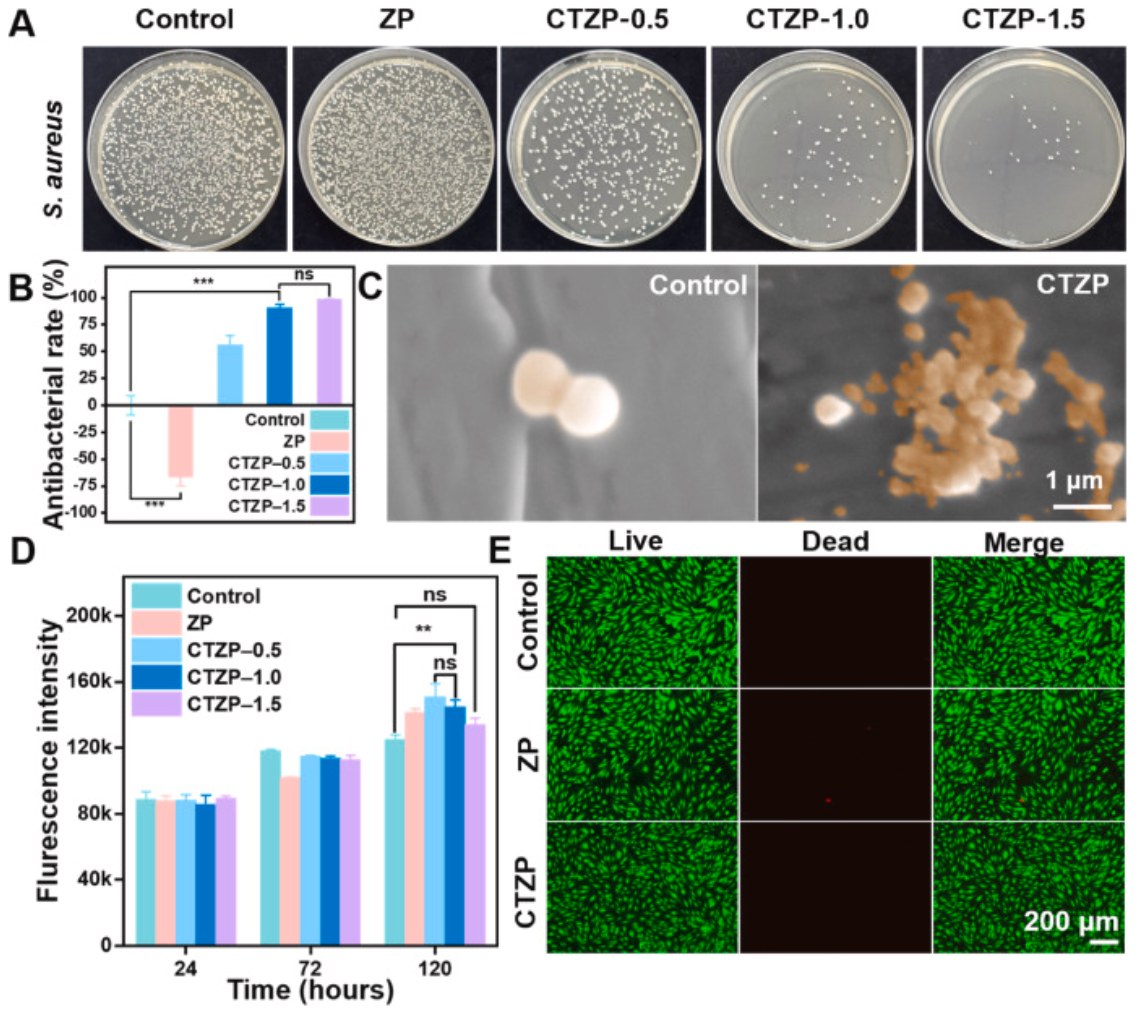
图3 ZP和CTZP的抑菌活性和细胞相容性。(A)对照、ZP、CTZP0.5、CTZP-1.0和CTZP-1.5中金黄色葡萄球菌菌落的代表性琼脂平板照片,(B)对应的金黄色葡萄球菌抑菌率。 (C)与CTZP-1.0或不与CTZP-1.0共培养的金黄色葡萄球菌的代表性形态。 (D) HUVECs与不同样品共培养24、72和120小时的细胞增殖情况。(E)与ZP和CTZP-1.0共培养24小时的HUVECs活细胞/死细胞染色荧光图像。
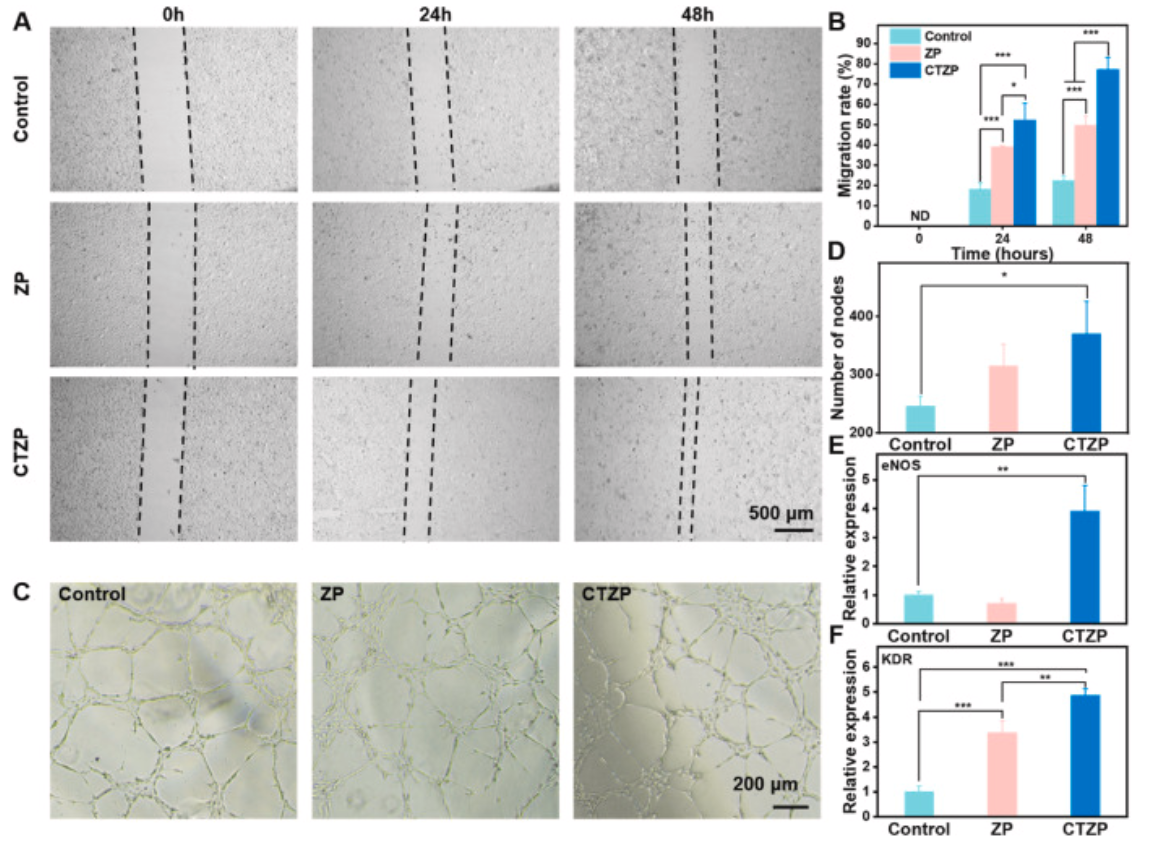
图4 细胞迁移和血管生成特性评价。L929的细胞迁移图像(A),以及对照、ZP和CTZP在24和48 h时细胞迁移率的定量分析(B)。对照组、ZP和CTZP在体外6 h HUVECs成管实验(C),以及相应的节点数定量分析(D)。血管生成相关基因的表达水平,包括内皮型一氧化氮合酶(eNOS)(E)和激酶插入结构域受体(KDR)(F)。

图5. CTZP促进体内感染伤口愈合。(A)体内实验示意图和原位静电纺丝CTZP在伤口部位,金黄色葡萄球菌感染1天后,在第0天原位加载纳米纤维敷料,然后在第1、4、7和14天收集大鼠皮肤组织。(B)原位静电纺丝CTZP前后的伤口照片。(C)对照、ZP和CTZP组第1天和第4天金黄色葡萄球菌的代表性琼脂板图像。对照组、ZP组和CTZP组(n = 4)伤口区域的代表性照片(D)和相应的伤口愈合率(E)。对照组、ZP组和CTZP组在第1、4、7和14天的代表性苏木精和伊红(H&E)染色图像(F),以及第14天相应的肉芽肿厚度(G)。对照、ZP和CTZP组第1天和第4天的Giemsa染色图像(H)和第7天和第14天的Masson三色染色图像(I)。 对照组、ZP组和CTZP组第14天VEGF和CD31的免疫组化染色图像(J),以及相应CD31 (K)和VEGF (L)的定量分析。
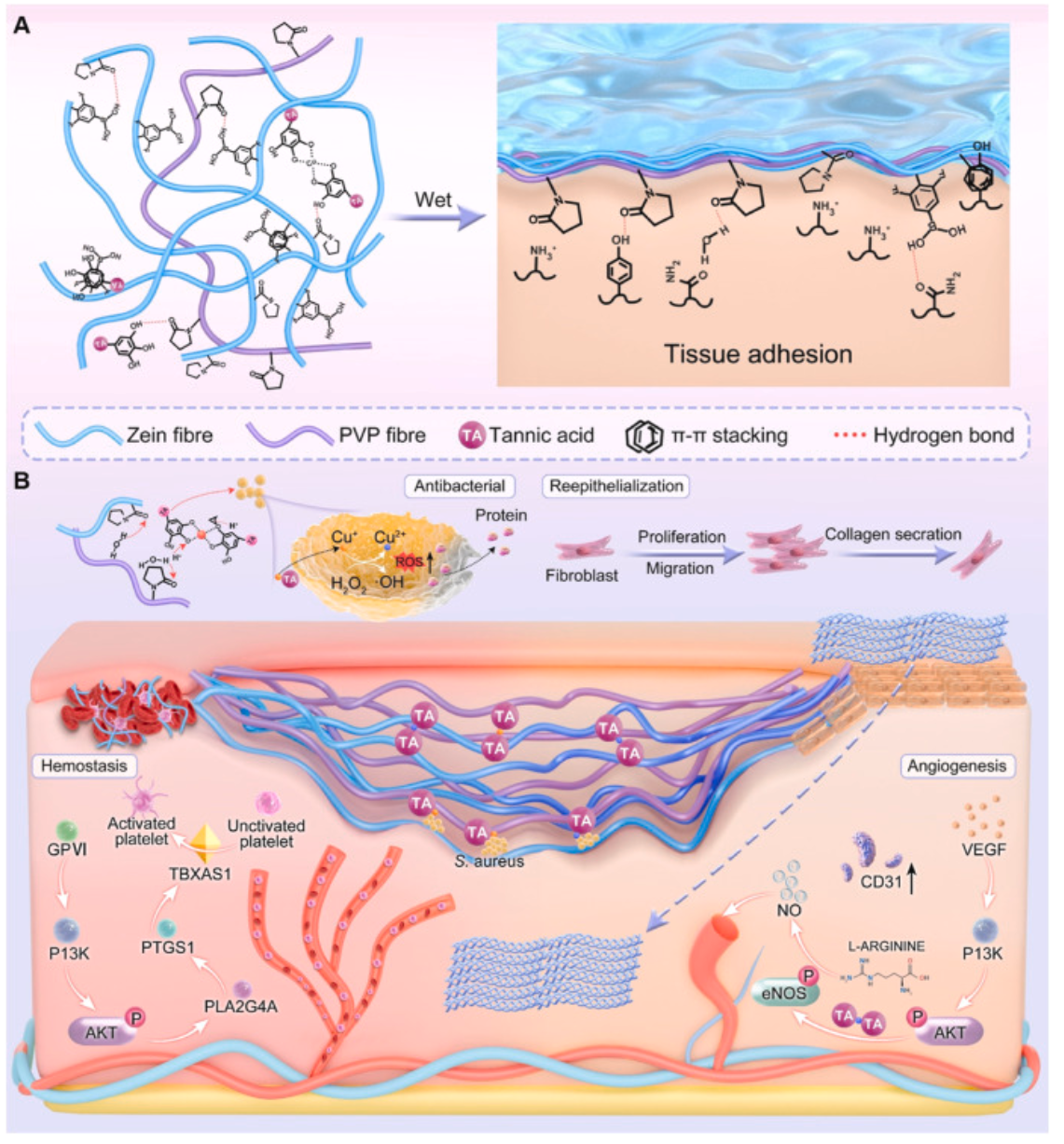
图6 CTZP的潜在作用机制。(A) Cu@TA、Zein和PVP在CTZP内的结构相互作用,以及CTZP可能的组织粘附机制。(B) CTZP通过止血、抗菌、再上皮化和血管生成加速伤口愈合的假设机制。
结论
综上所述,本文提出了一种由玉米蛋白/PVP和Cu@TA纳米颗粒组成的原位电纺丝CTZP纳米纤维敷料。采用医用消毒酒精作为绿色溶胶孔,既消除了有机溶胶孔的风险,又简化了材料制备过程,便于便携式静电纺丝的实际应用。生物相容性CTZP纳米纤维敷料通过高表达的TBXAS1激活血小板,表现出快速止血性能。从机制上讲,Cu@TA NPs一方面促进了ZP内在的VEGF促进能力,另一方面,它们赋予了eNOS调控活性,可以协同促进血管生成。有趣的是,血小板活化和VEGF信号通路都是由高表达的PI3K-Akt信号通路介导的。此外,Cu@TA NPs的掺入赋予了有效的抗菌活性并增强了成纤维细胞的活性。本研究为便携式原位静电纺丝止血、抗菌、促血管生成敷料用于急性创面即时治疗提供了理论和物质基础。
原文链接:https://doi.org/10.1016/j.bioactmat.2025.08.020
