伤口愈合是一个系统而复杂的过程,涉及影响伤口修复不同阶段的各种内在和外在因素。因此,能够调节这些因素以促进伤口愈合的多功能伤口敷料需求量很大。
近期,广东工业大学汤亚东副教授和广东省科学院高博韬研究员通过在亲水性聚(ε-己内酯)@聚多巴胺-ε-聚赖氨酸(PCL@PDA-ε-PL)纳米纤维膜上沉积同轴纳米纤维,制备了一种具有抗菌抗炎、药物控释和单向水传输特性的多功能Janus静电纺丝纳米纤维敷料。该同轴纳米纤维壳层中负载有相变材料月桂酸(LA),核层中负载有抗炎布洛芬(IBU)。其中,熔点为43℃的LA作为相变材料控制IBU的释放。近红外(NIR)辐照诱导LA的相变,从而触发PDA的光热特性。由于PDA的光热特性和ε-PL的抗菌特性,Janus纳米纤维敷料对大肠杆菌和金黄色葡萄球菌具有协同抗菌性能。所制备的Janus纳米纤维敷料还表现出抗炎活性和生物相容性。此外,Janus纳米纤维敷料还具有不对称的润湿性,能够实现水的定向输送,从而排出过量的伤口渗出液。水蒸气传输测试表明,Janus纳米纤维敷料具有良好的透气性。最后,对大鼠皮肤伤口愈合的评估证实了它在促进伤口愈合方面的功效。因此,这种设计和制造多功能Janus纳米纤维敷料的策略在伤口愈合应用中具有巨大潜力。
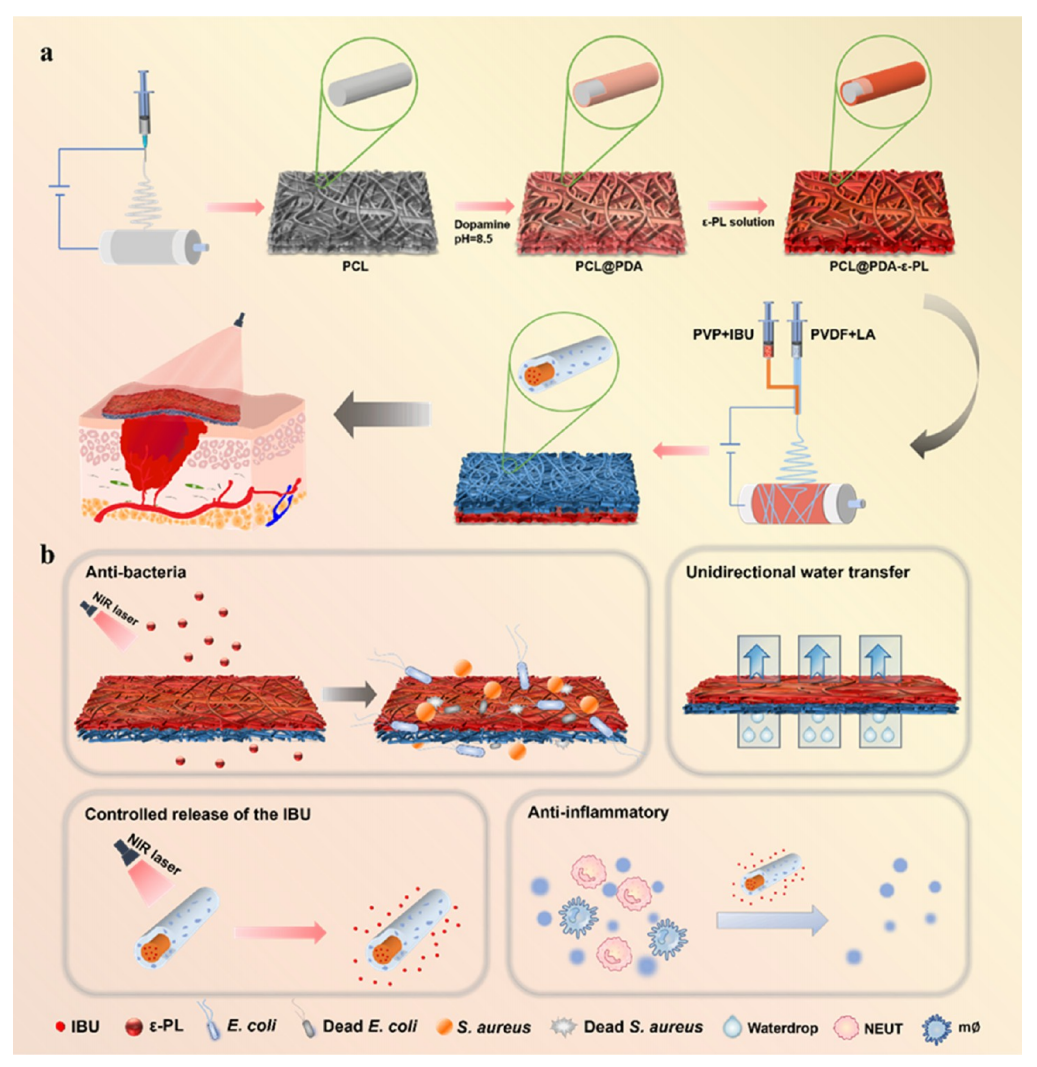
图1.(a)Janus复合纳米纤维膜的制备示意图。(b)所制备的Janus复合纳米纤维膜具有抗菌、药物控释、抗炎和定向输水等多功能特性。
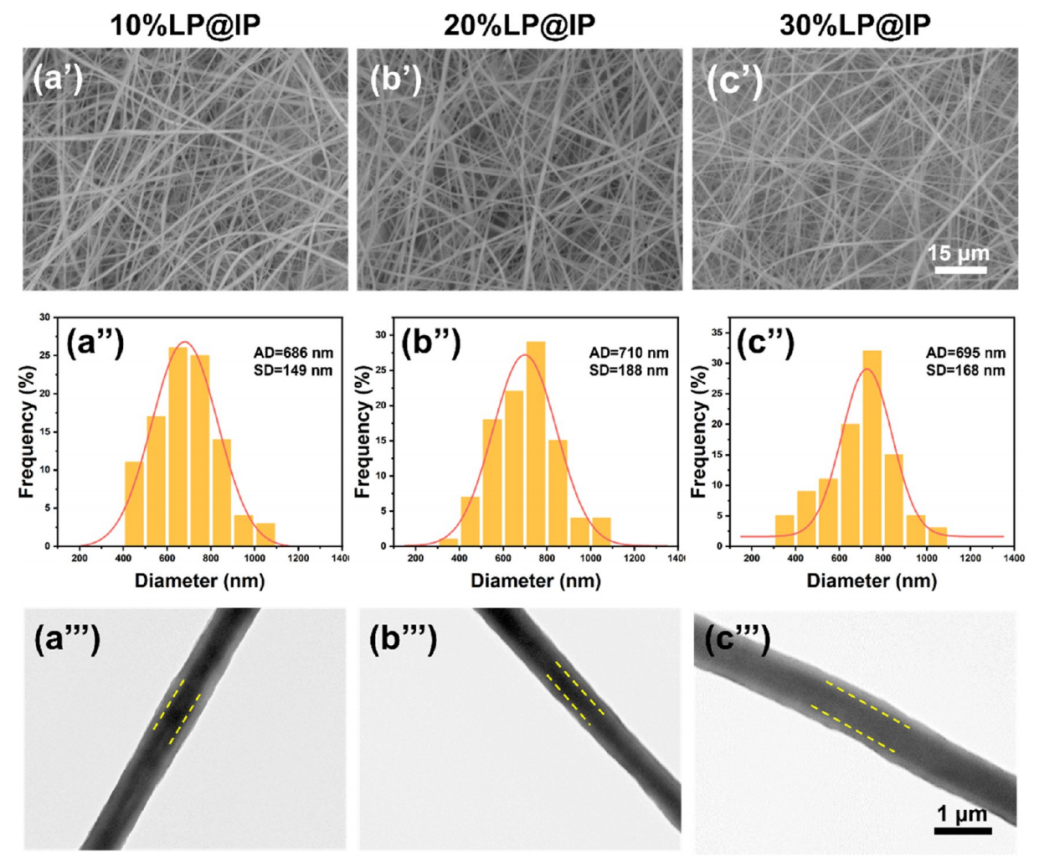
图2.同轴纳米纤维的SEM形态、直径分布和TEM图像。
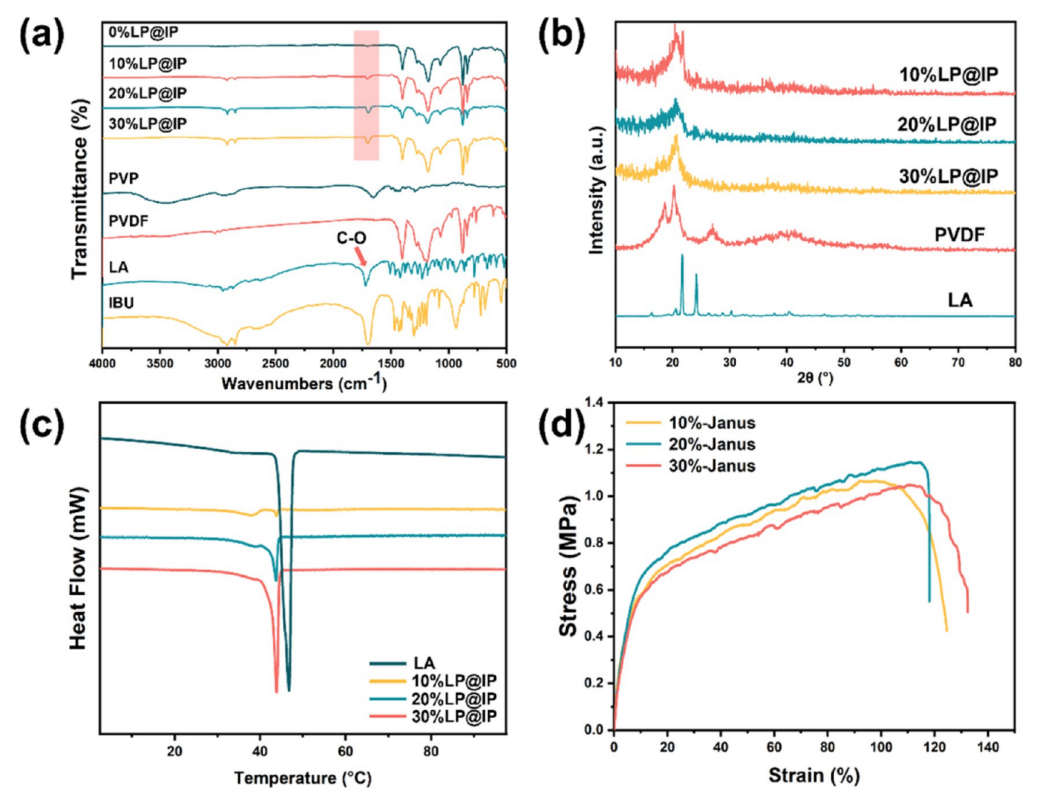
图3.(a)ATR模式下同轴纳米纤维膜和透射模式下原材料(PVP、PVDF、LA和IBU)的FTIR光谱。(b)同轴纳米纤维膜和原材料(PVP、PVDF和LA)的XRD光谱。(c)同轴纳米纤维和纯LA的DSC热谱图。(d)Janus复合纳米纤维膜的应力-应变曲线。
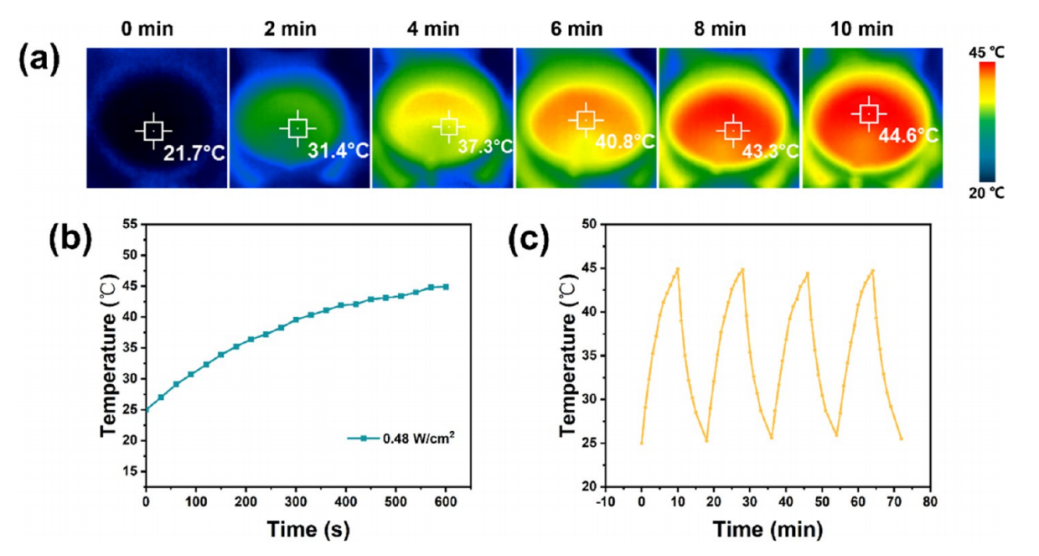
图4.(a)使用808nm激光照射的Janus复合纳米纤维膜的红外热成像。(b)Janus复合纳米纤维膜随辐照时间的温度变化。(c)Janus复合纳米纤维膜的近红外光热响应稳定性。
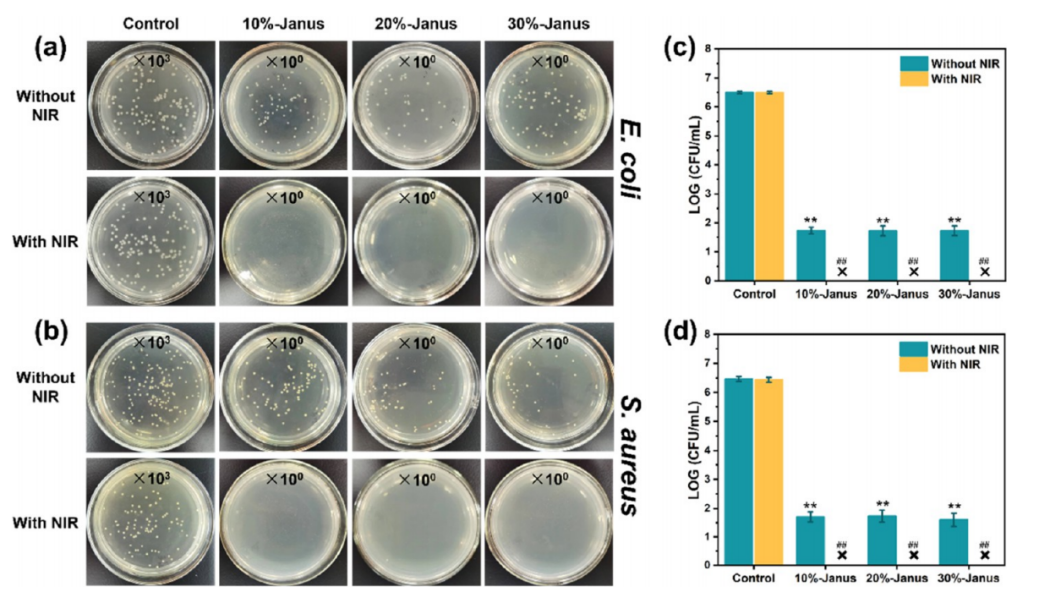
图5.(a,b)经或未经808nm NIR辐照10分钟的情况下,对照(盐水溶液)、10%-Janus、20%-Janus和30%-Janus复合纳米纤维膜组中大肠杆菌(a)和金黄色葡萄球菌(b)菌落的照片。(c,d)根据平板涂布法计算的大肠杆菌(c)和金黄色葡萄球菌(d)的菌落计数。与对照组相比,**p<0.01。与无激光辐照组相比,##p<0.01。
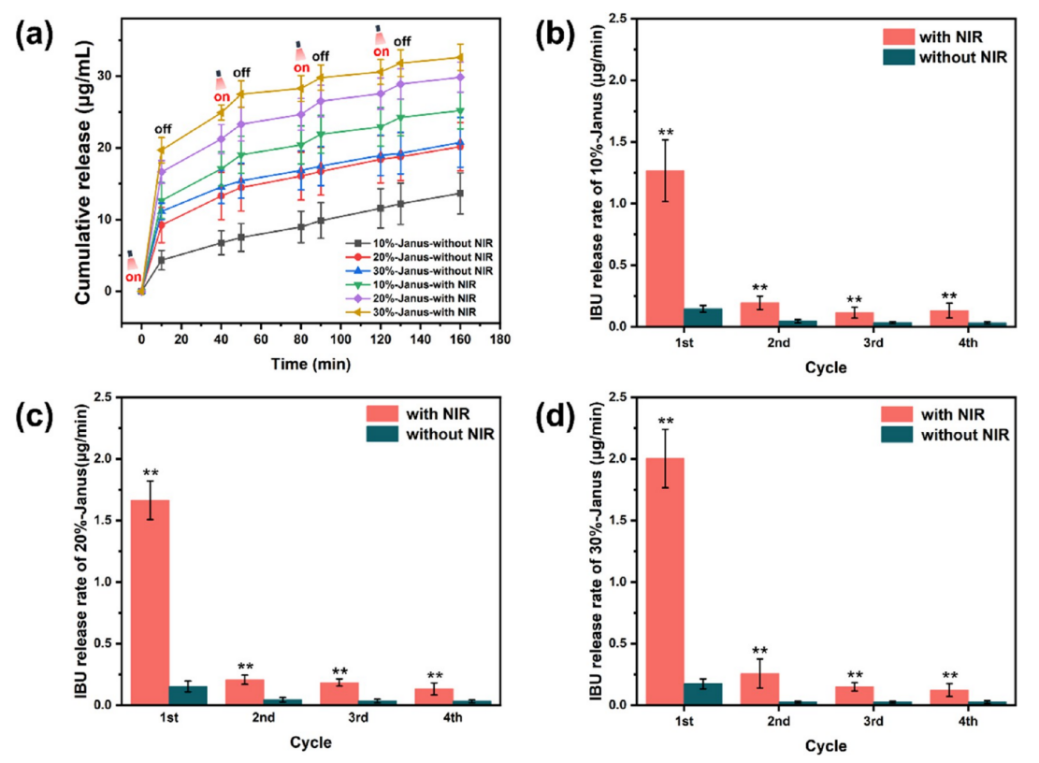
图6.(a)四个激光辐照循环后,Janus复合纳米纤维膜的IBU累积释放量。(b-d)10%-Janus(b)、20%-Janus(c)和30%-Janus(d)Janus复合纳米纤维膜的IBU释放率。与无激光辐照组相比,**p<0.01。
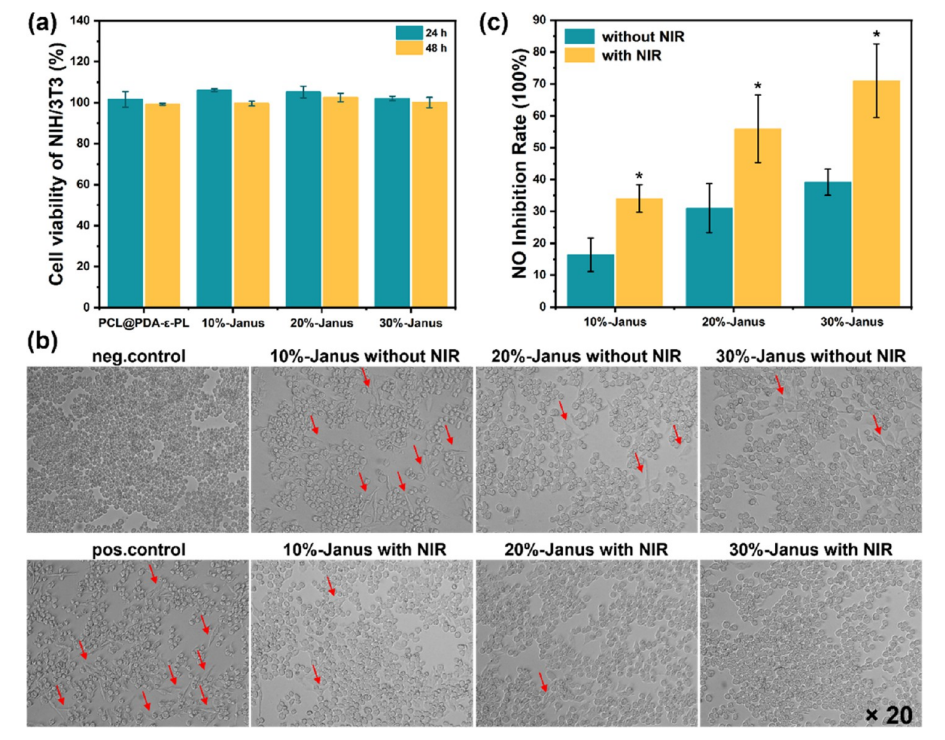
图7.(a)NIH/3T3细胞的细胞活力。(b)RAW 264.7细胞的相差显微镜图像(红色箭头表示纺锤形细胞)。(c)通过Griess法测定Janus复合纳米纤维膜的NO抑制率。与无激光辐照组相比,*p<0.05。
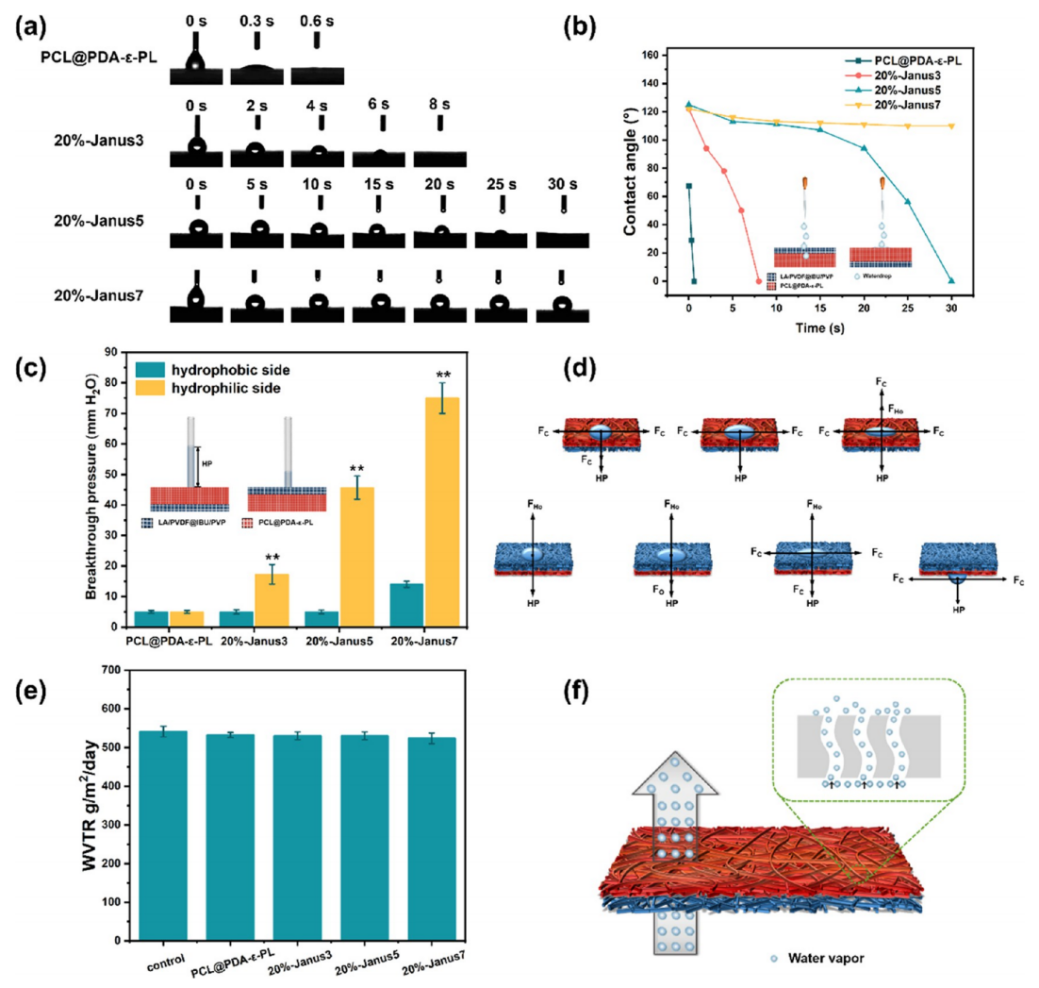
图8.PCL@PDA-ε-PL、20%-Janus3、20%-Janus5和20%-Janus7纳米纤维膜的WCA图像(a)、WCA变化曲线(b)和穿透压力(c)。(d)Janus复合纳米纤维膜的单向水传输机制(FC:毛细管力;HP:基于每单位液滴的质量;FHo:疏水层的疏水性)。(e)WVTR的示意图。(f)PCL@PDA-ε-PL、20%-Janus3、20%-Janus5和20%-Janus7纳米纤维膜的WVTR。与疏水侧方向的穿透压力相比,**p<0.01。
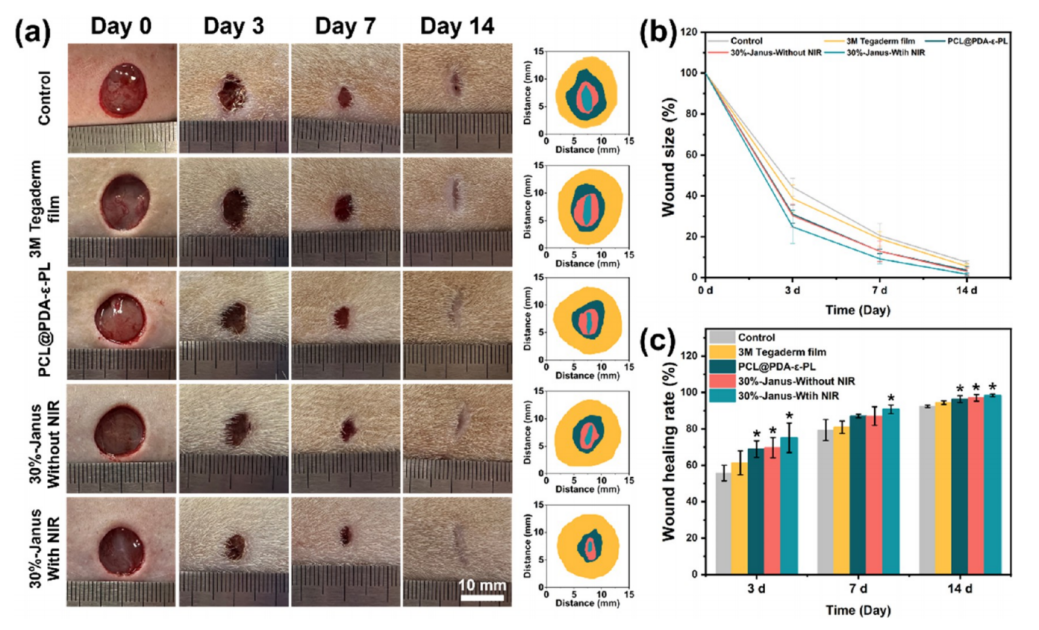
图9.纳米纤维支架的体内伤口愈合研究。
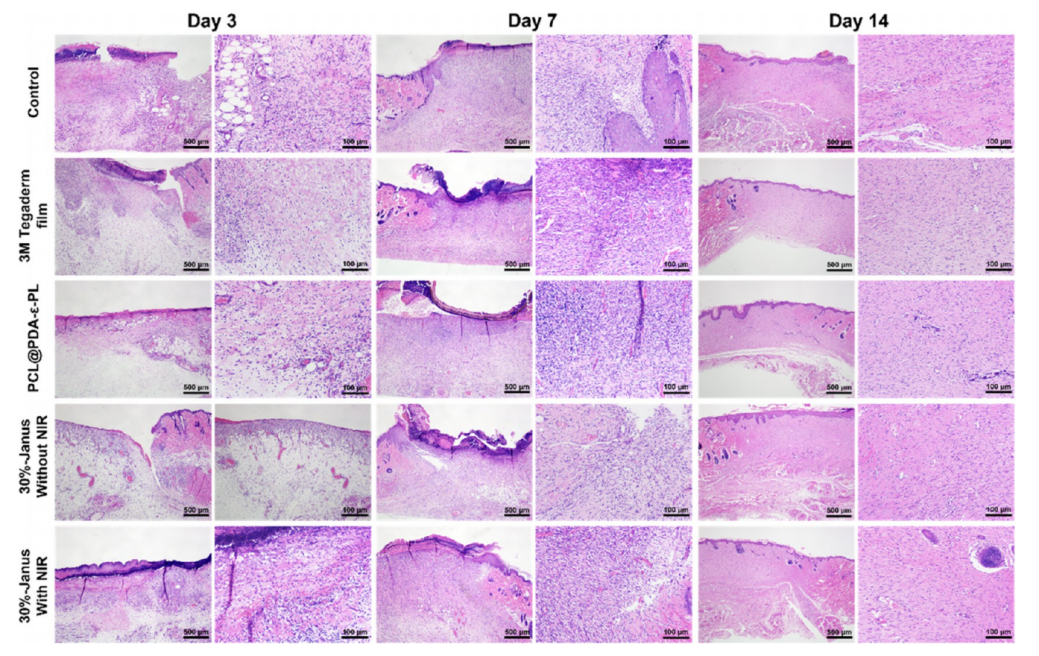
图10.经不同材料处理后第3、7和14天再生皮肤组织的H&E染色切片。
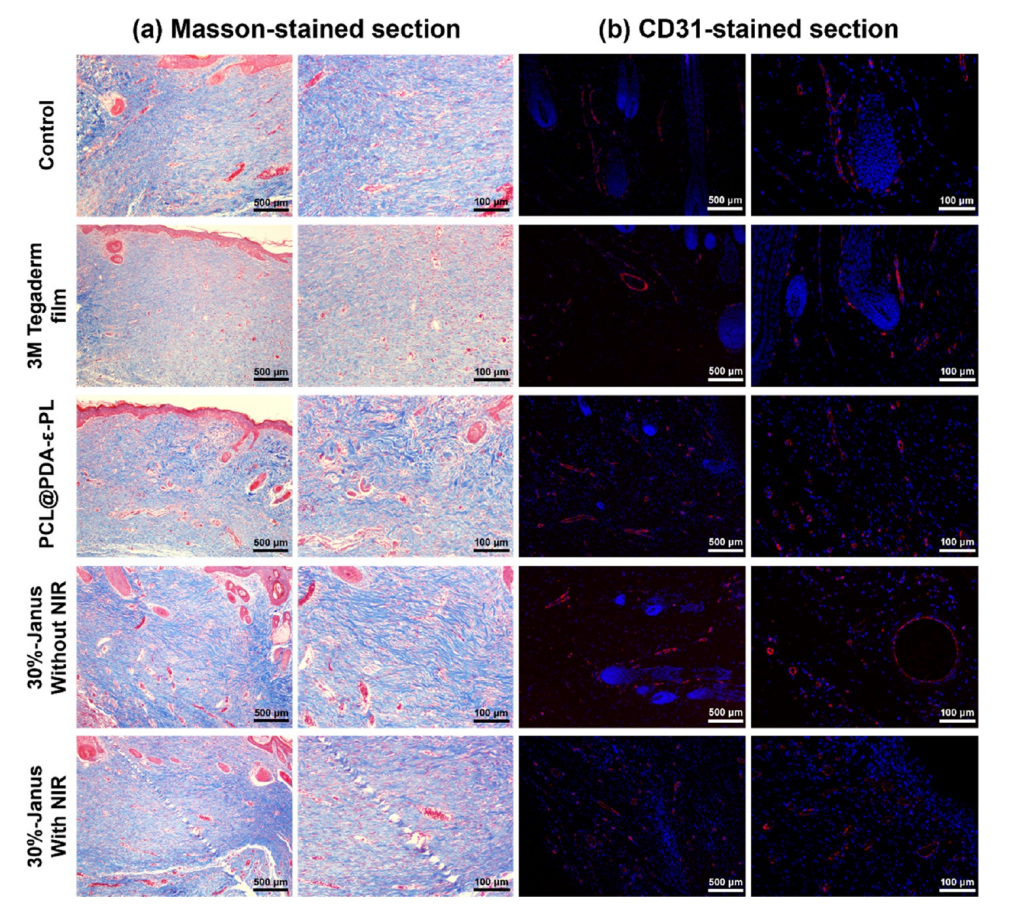
图11.(a)经Masson染色的再生皮肤组织切片图像。(b)经不同组处理后第14天再生组织的CD31染色切片(蓝色,细胞核;红色,CD31)。
该工作以“Phase Change Material-Embedded Multifunctional Janus Nanofiber Dressing with Directional Moisture Transport, Controlled Release of Anti-Inflammatory Drugs, and Synergistic Antibacterial Properties”为题发表在《ACS Applied Materials & Interfaces》(DOI:10.1021/acsami.3c11903)上。
论文链接:https://doi.org/10.1021/acsami.3c11903
