口服给药是最常见和最方便的给药途径,结肠靶向或结肠特异性给药在实验室研究和工业生产中已经持续了多年。具有不同作用机制的新材料不断被开发。其中,pH敏感聚合物基于其pH溶解度依赖性,可以利用其pH敏感特性准确地实现药物的结肠靶向。这些聚合物在胃中不溶,但在中性条件下可溶。虽然许多研究已经证明了pH敏感给药系统(DDS)的可行性,但很少有报道关注结肠停留时间对有效药物吸收的影响。由于结肠的特殊环境,在该区域释放的药物经常受到结肠内食物内容物的碰撞和挤压,这可能进一步导致药物释放紊乱。因此,一种理想的口服结肠靶向DDS不仅要对胃肠道酶和水解降解具有较强的稳定性,还要具有一定的结肠粘附能力,以确保其与结肠粘膜接触时间更长,吸收能力更强。

近日,上海理工大学材化学院余灯广教授团队、上海市市东医院刘萍教授团队以及海军医科大学海军医学中心皮肤科朱元杰教授团队联合在国际知名期刊《Advanced Composites and Hybrid Materials》,发表了最新研究成果“Electrospun Janus core (ethyl cellulose//polyethylene oxide) @ shell (hydroxypropyl methyl cellulose acetate succinate) hybrids for an enhanced colon targeted prolonged drug absorbance”。该成果第一作者为博士生周建锋同学。余灯广教授、刘萍教授和朱元杰教授为共同通讯作者。研究者通过静电纺丝技术以三种聚合物,pH敏感材料HPMCAS、生物黏附材料PEO和惰性材料EC,以及一种模型药物5-氟尿嘧啶制备了Janus core@shell (JCS)杂化纳米结构。结合材料与生物环境的特点,模型药物被合理设计到纳米纤维中,实现高效结肠靶向药物递送。
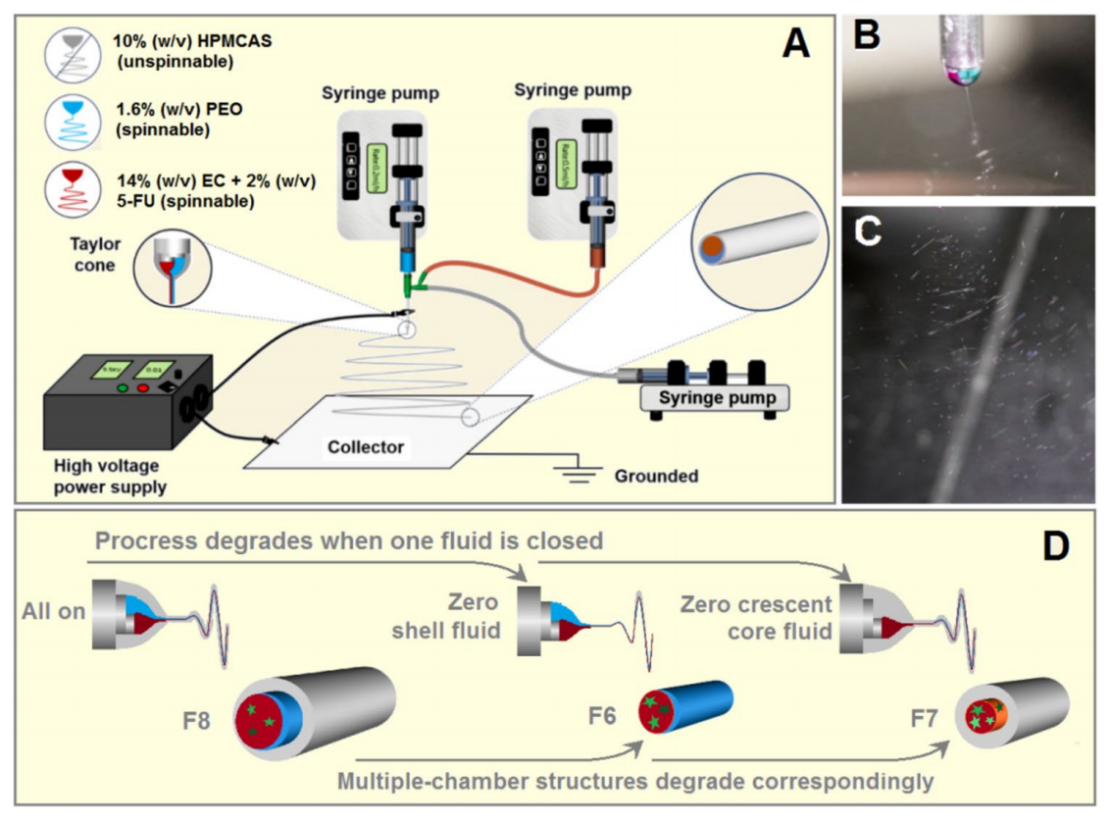
图1:静电纺丝过程:A)用于构建JCS纳米纤维F8的三流体静电纺丝示意图;B和C)分别是复合泰勒锥以及弯曲鞭动区域的照片。D)关于三流体静电纺丝降级为双流体过程以及JCS结构相应转变为Janus核壳结构的示意图。
如图1所示,利用自制偏心针头,实施并行电纺技术、制备出双层核壳纳米纤维F6和F7以及Janus core@shell (JCS)杂化纳米结构F8。

图2:纳米纤维的SEM和TEM图像以及直径分布:A和D)F6;B和E)F7;以及C和F)F8。
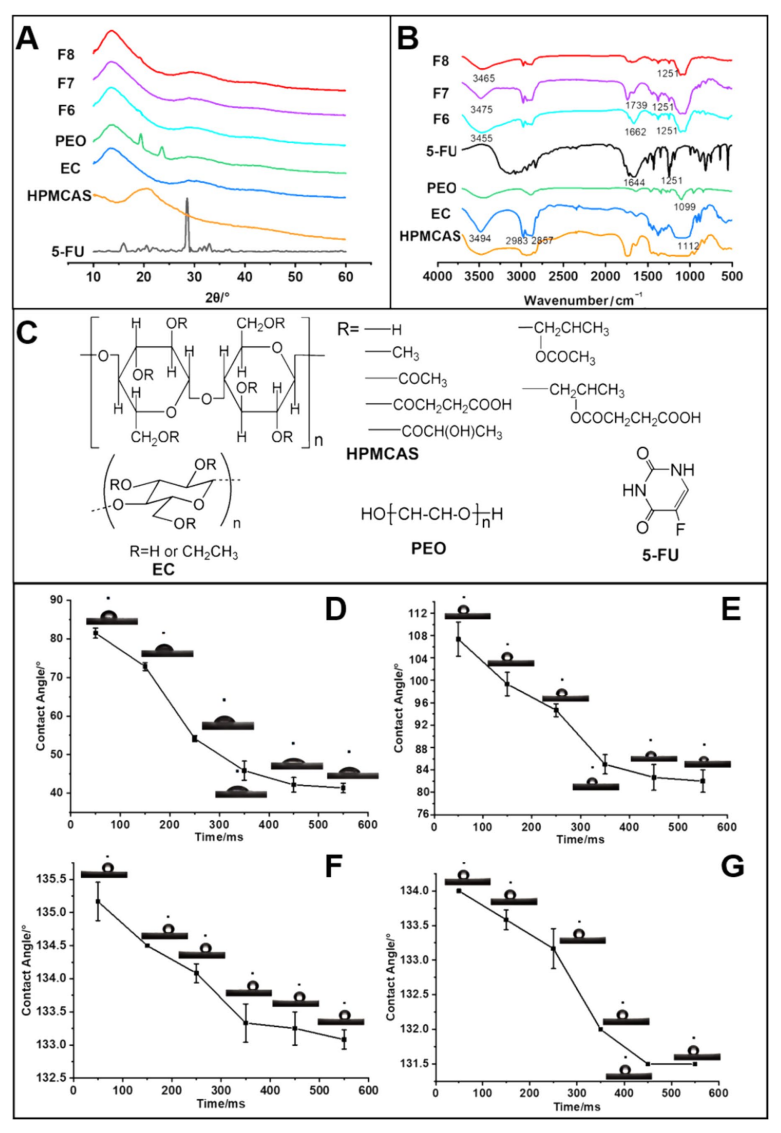
图3:物理状态、相容性和亲水性:A)XRD图谱;B)FTIR光谱;C)分子式;D-G)F3、F6、F7和F8的动态水接触角。
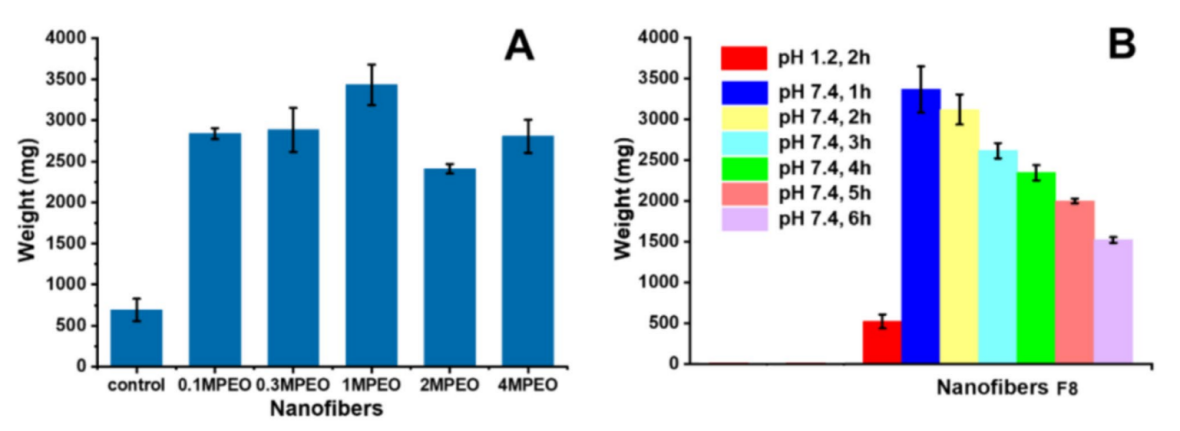
图4:粘膜粘附测试结果:A)不同分子量的PEO纳米纤维(空白作为对照)和B)在不同条件下处理的纳米纤维F8。
如图4A所示,采用单流体静电纺丝法制备了不同分子量的PEO纳米纤维。结果表明,无论PEO的分子量如何,纤维对猪结肠的年负能力都显著增加,其中1 M的PEO纤维薄膜的粘附性能最强。图4B探究了JCR纳米纤维的粘附能力,结果显示,盐酸缓冲液浸泡的F8不具备黏附能力,PBS(pH 7.4)缓冲液浸泡的F8的结肠黏附能力随浸泡时间的延长而减弱。
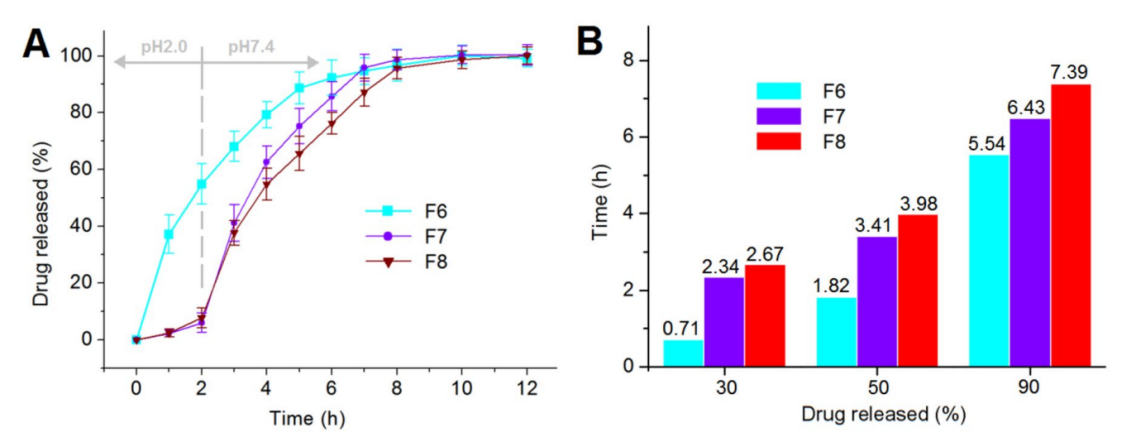
图5:体外溶出曲线:A)纳米纤维F6-F8的累积药物释放曲线,B)F6-F8达到一定药物释放百分比所需的时间。
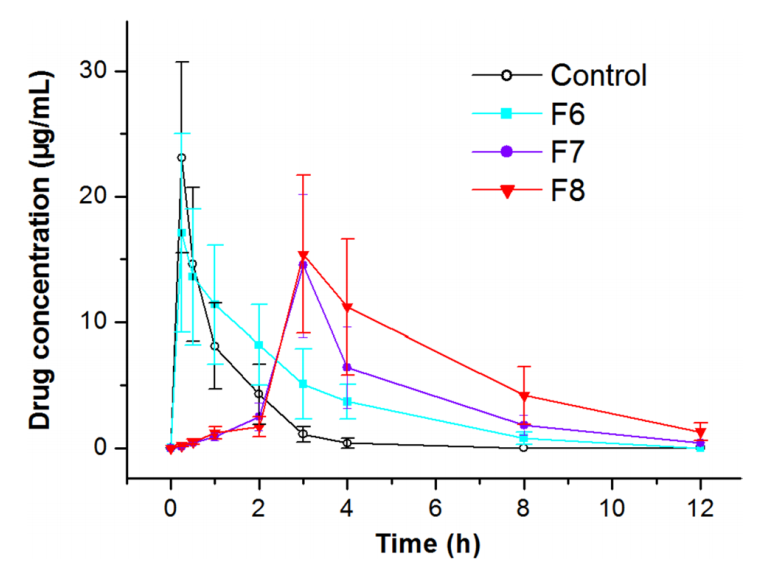
图6:SD大鼠口服游离药物和三种不同纳米纤维制剂后的血浆药物浓度时间分布。
如图6所示,与5-FU溶液相比,F6、F7和JCS纤维F8的AUC0-t分别增强了2.47倍、2.91倍和3.97倍。同样,F6、F7和F8的AUC0-∞的改善率分别为2.42倍、2.87倍和3.85倍。这些结果表明,药物吸收的改善作用和口服生物利用度的增加遵循F8>F7>F6的顺序。JCS纳米结构比双层Janus和核壳纳米结构进一步促进了药物的吸光度。
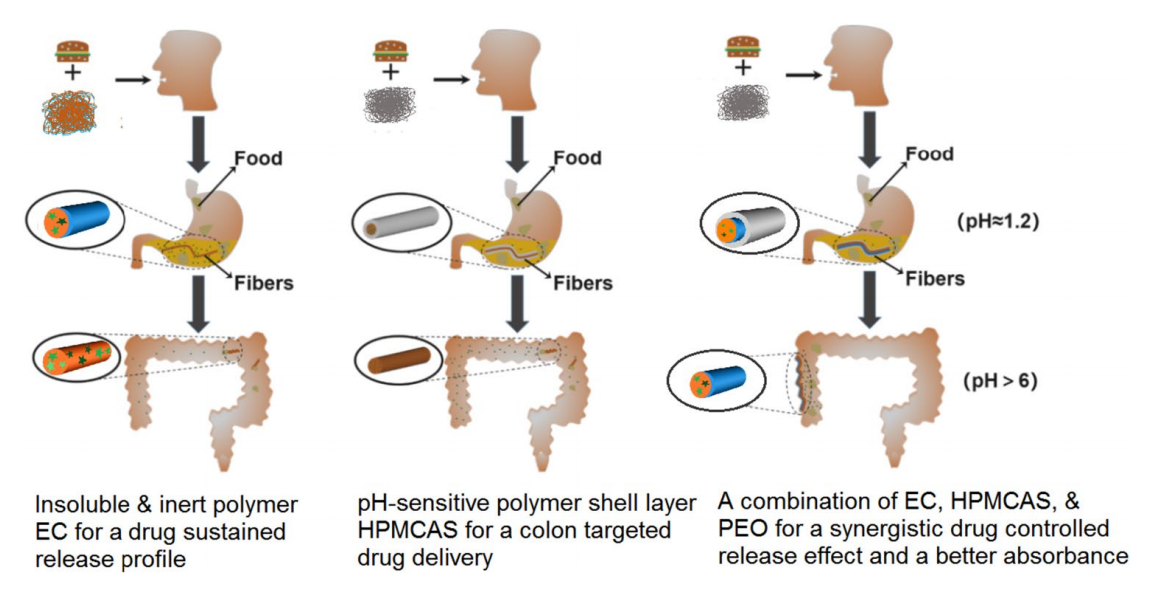
图7:不同结构性质的比较,揭示了Janus核壳纳米结构提高药物吸收率的机理。
图7为Janus核壳纳米结构提高药物吸收率的机理。口服F6后,在胃的酸性环境中释放了大量的药物,只剩余的少量药物被释放出来且会受到内容物的影响,导致药物释放不稳定。PEO侧虽然是可溶性聚合物,但也可以通过,(1)减少直接接触体液的初始载药表面和(2)阻断或阻止水分子在纳米纤维中的渗透和药物分子的扩散路线,使纳米纤维留在两侧的界面上。F7由于HPMCAS的覆盖,具有抵抗酸性环境的能力,使其可以通过胃区并将大部分负载的5-FU在结肠区域释放。当EC-药物核心被EC-药物//PEO Janus核心取代时,PEO侧会促进EC-药物在结肠黏膜上的附着,从而进一步提高5-FU的吸光度。因此,通过三种不同聚合物的分阶段协同作用,保证了5-FU在结肠区域的缓释和良好的吸光度。
该研究策略包含了一个有趣的指导,通过先进的技术探索不同种类的聚合物在纳米尺度上的有意安排,以增强协同剂的功能性能。正如本研究所揭示的那样,在给药领域,药物设计直接关系到最终剂型的质量,因此组织成分的策略非常重要。聚合物和先进技术的结合可以有效地丰富开发新型纳米药物传递系统。基于本文的研究,制备的JCS纳米结构可以作为一个强大的平台,支持各种新型功能纳米材料的开发。
论文链接:https://doi.org/10.1007/s42114-023-00766-6
人物简介:
余灯广,研究员,上海理工大学教授,博士生导师,主持国家自然科学基金项目2项(含1项中英国际合作互访项目)、上海市自然科学基金、上海市教委科研创新重点项目、中国博士后第二批特别资助等科研项目。在《Applied Catalysis B: Environmental》、《Chemical Engineering Journal》、《Journal of Controlled Release》、《Advanced Fiber Materials》、《Macromolecules》等国内外杂志发表学术论文300余篇,其中被SCI收录论文250余篇,1% ESI高被引64篇,0.1%热点论文27篇,2020年, 2021年,2022年Elsevier高被引学者,H-index=64。申请国家发明专利80余项,已授权40余项。指导本科生获得“挑战杯”国赛、市赛等各类奖项10余次,获得上海市“育才奖”和上海市教学名师称号。
