DOI: 10.3390/pharmaceutics13040556
在本研究中,以聚乙烯吡咯烷酮为聚合物基体,采用低成本静电纺丝法以无定形固体分散体的形式制备了水溶性较差的抗生素环丙沙星(CIP)纳米纤维。纳米纤维的溶解度及其体外扩散均显著高于CIP粉末或两种组分的物理混合物。对纤维的尺寸和形态进行了优化,发现向静电纺丝溶液中添加CIP会降低纳米纤维的直径,从而使比表面积增加。结构表征证实了药物与聚合物之间的相互作用以及纳米纤维内部CIP的无定形状态。由于CIP的溶解度具有pH依赖性,因此在不同的pH值下进行了体外溶解度和溶出度研究。具有最佳形貌的纳米纤维样品在水和pH7.4缓冲液中的溶解度均显著增加。进行了单介质和两阶段生物相关溶出研究,并通过数学模型阐述了释放机理。此外,与纯药物和物理混合物相比,pH6.8到pH7.4条件下的体外扩散显著增加。环丙沙星负载聚乙烯吡咯烷酮(PVP)纳米纤维是一种具有良好物理化学性质的速溶制剂。

图1.环丙沙星负载纳米纤维的制备。
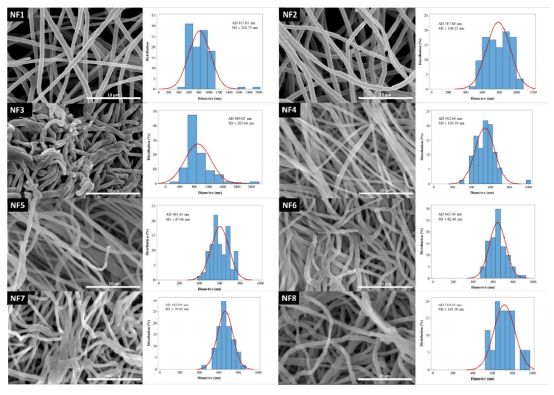
图2.纳米纤维样品的SEM图像和直径分布(放大5000倍)。
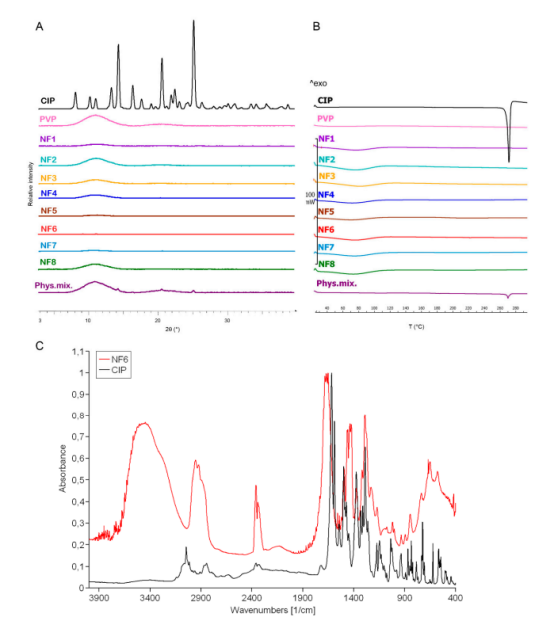
图3.环丙沙星(CIP)、PVP、物理混合物和NF1-NF8纳米纤维样品的XRPD衍射图(A)和DSC热谱图(B)。所有的静电纺丝样品均为无定形固体分散体。CIP和NF6纳米纤维样品的FTIR光谱(C)。观察到的位移和加宽证实了CIP成功掺入聚合物纤维中。
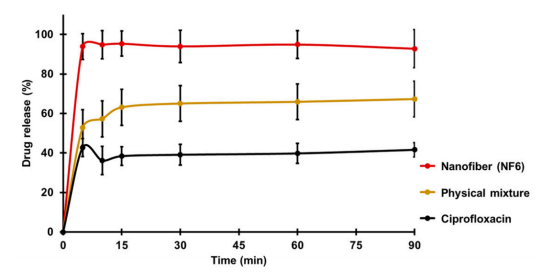
图4.在pH7.4的磷酸盐缓冲液中,NF6纳米纤维、物理混合物和CIP粉末的环丙沙星(CIP)体外溶出。所有测得的NF6值均显著高于原始CIP值(p<0.001),而前两个值均显著高于物理混合物值(p<0.05)。统计分析:两样本t检验。
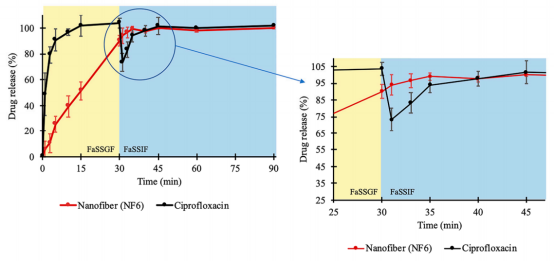
图5.在两阶段生物相关释放研究中,NF6纳米纤维和CIP粉末的环丙沙星(CIP)体外溶出。溶出介质(FaSSGF)模拟胃部条件,直到30分钟后该介质变为FaSSIF生物相关流体。放大介质变化的时间范围(25-45分钟),以便更好地观察。
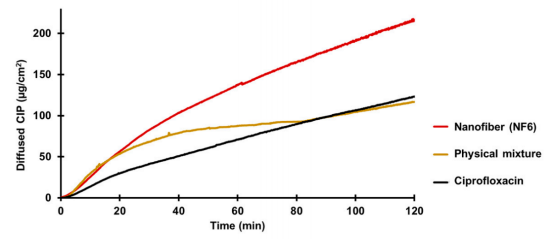
图6.NF6纳米纤维样品、物理混合物和CIP粉末的环丙沙星体外扩散(SD±2%)。
