DOI:10.1016/j.ijbiomac.2020.07.278
在这项工作中,研究者提出了一种实现α-淀粉酶和辣根过氧化物酶(HRP)双重固定化的简便技术,即通过简单的混合步骤,将两种不同的酶模型包封在两种不同的聚合物电纺纤维中,并比较它们在单独固定化形式和游离形式下的性能。使用傅里叶变换红外光谱(FTIR)和场发射扫描电子显微镜(FESEM)对固定化进行了验证。双固定化HRP和α-淀粉酶的固定化效率分别为89%和85%。双固定化HRP和α-淀粉酶在10个循环后的催化活性分别为79%和80.2%。储存12周后,双重固定化酶仍保留与单独固定化酶相似的活性,接近于90%。相对于不同的酶活性测定方法,该固定方法似乎对两种酶均未产生负抑制或反抑制作用。这种方法表明,两种或多种类型的酶可以分别与不同的聚合物混合,并同时进行静电纺丝。作者认为该方法有望大大促进和扩展多酶系统的应用,同时为酶介导级联反应的深入研究奠定了坚实的基础。
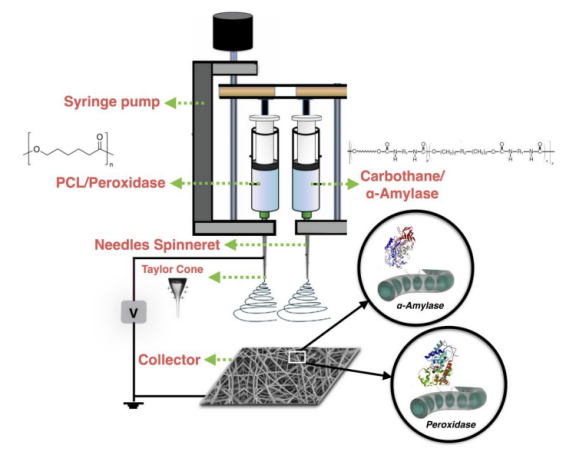
图1.酶(HRP和α-淀粉酶)的双重固定化过程。

图2.含α-淀粉酶和HRP的电纺纤维的FESEM图像。
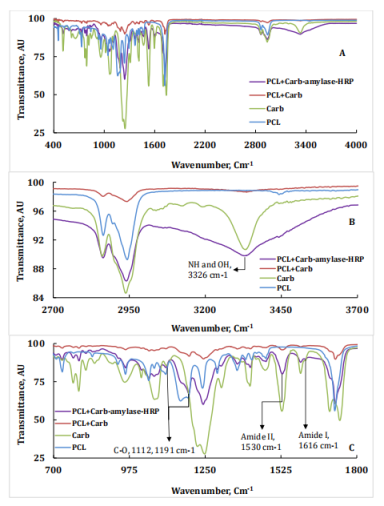
图3.PCL(PCL),聚碳酸酯基聚氨酯(Carb),PCL与聚碳酸酯基聚氨酯(PCL/Carb)以及封装α-淀粉酶和辣根过氧化物酶的PCL与聚碳酸酯基聚氨酯(PCL/HRP+Carb/淀粉酶)的ATR-FT-IR光谱(A)和扩展区域的ATR-FT-IR(B,C)。
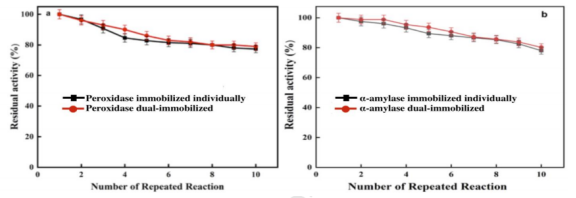
图4.单独和双重固定化HRP(a),单独和双重固定化α-淀粉酶(b)的再利用。每个点代表三次实验的平均值±SE。
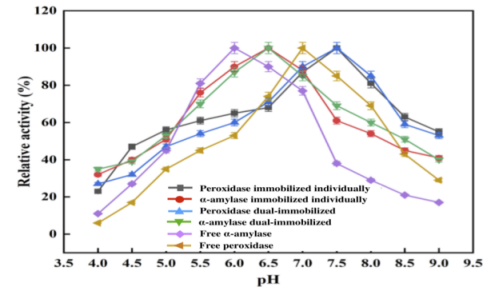
图5.pH的影响。
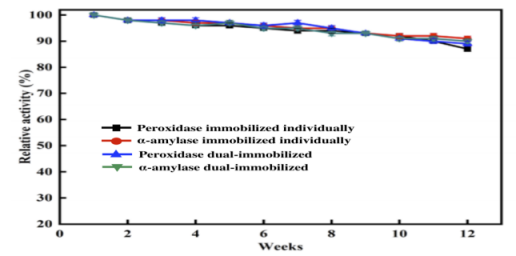
图6.在4℃下的存储稳定性。
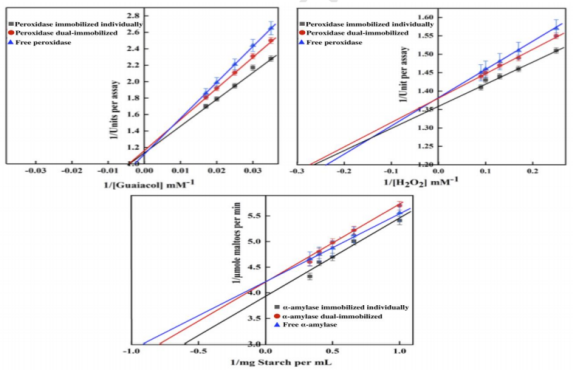
图7.(a)愈创木酚和(b)H2O2浓度下过氧化物酶活性以及(c)淀粉存在下α-淀粉酶活性的Lineweaver-Burk图和底物饱和曲线。
