DOI: 10.1002/adhm.202000200
神经引导管(NGC)在修复周围神经损伤方面具有替代自体移植物的潜力,但其疗效仍有待提高。促进轴突生长的神经营养因子和能够降解抑制轴突生长的分子的酶增强了NGC的疗效。在当前研究中,构建了两种负载因子(神经营养因子-3和软骨素酶ABC)的NGC,并考察了它们修复大鼠坐骨神经8 mm间隙的能力。这些因子被封装在由相变材料(PCM)或胶原蛋白制成的微粒中,然后夹在两层电纺纤维之间。使用PCM可以在用近红外激光照射时实现因子的脉冲释放。使用胶原蛋白可以通过扩散实现缓慢、连续的释放。通过测定腓肠肌中的复合肌肉动作电位(CMAP)并分析神经组织学来评估其疗效。胶原蛋白中因子的连续释放导致远端神经相对于普通导管的CMAP幅度增大,轴突数量增加。相反,来自PCM的相同因子的脉冲释放对疗效有明显的不利影响,这可能是通过抑制轴突生长引起的。

图1.A)沉积在单轴定向纤维表面的胶原蛋白颗粒的SEM图。B)含胶原颗粒因子负载导管中NT-3的累积释放特征。C)从含胶原蛋白因子负载导管中释放出的被ChABC消化的得体蛋白的百分比。误差棒代表一个标准偏差。
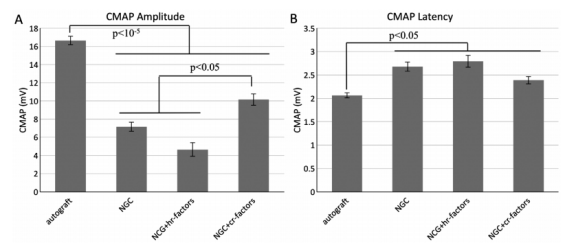
图2.每只动物的最大CMAP振幅和CMAP潜伏期(每组N=12),数据表示为平均值±平均值的标准偏差。A)自体移植导致相对于所有NGC组明显更高的CMAP幅度。接受NGC+cr因子的动物的幅度明显高于接受普通NGC或NGC+hr因子的动物。B)自体移植组的CMAP潜伏期明显短于任何导管组(p<0.05)。
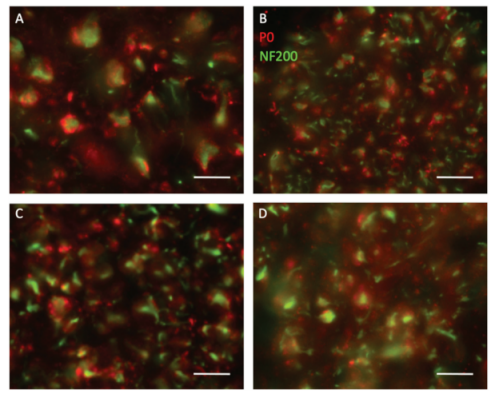
图3.髓磷脂和神经丝的免疫荧光染色。每组4到6只动物,获得20 µm冰冻切片,并用髓磷脂蛋白0(P0,红色)和神经丝200(NF200,绿色)的抗体染色。荧光显微照片显示了A)自体移植、B)普通NGC、C)NGC+hr因子和D)NGC+cr因子中点的代表性切片。在整个移植物和NGC中发现了被P0+髓鞘包围的NF200+轴突。两组之间未观察到总体差异。比例尺代表11.25 µm。
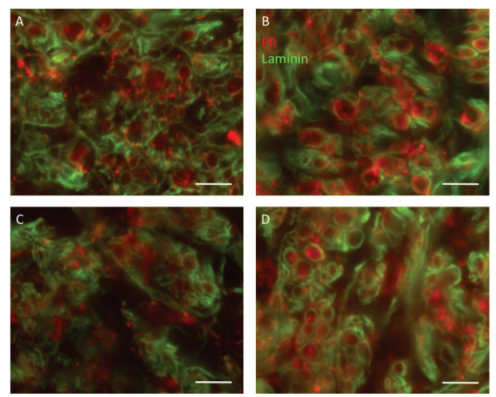
图4.髓磷脂和层粘连蛋白的免疫荧光染色。每组4到6只动物,获得20 µm冰冻切片,并用髓磷脂蛋白0(P0,红色)和层粘连蛋白(绿色)的抗体染色。荧光显微照片显示了A)自体移植、B)普通NGC、C)NGC+hr因子和D)NGC+cr因子中点的代表性切片。有髓鞘的轴突被形成基底膜的层粘连蛋白环包围。两组之间未观察到总体差异。比例尺代表11.25 µm。
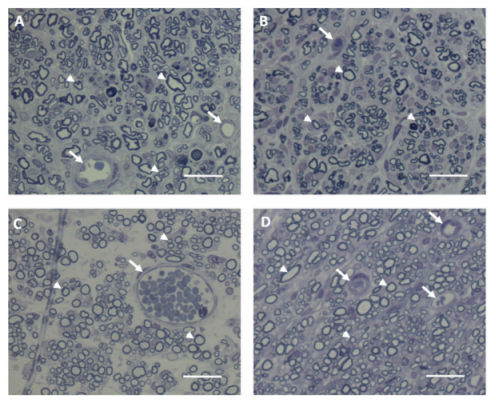
图5.半薄切片的组织化学分析。每组4到6只动物,组织用四氧化锇染色。得到0.7μm厚的切片,并用甲苯胺蓝复染。显微照片显示了A)自体移植、B)普通NGC、C)NGC+hr因子和D)NGC+cr因子中点的代表性切片。所有动物均显示有髓鞘的轴突(三角)和血管(箭头)。(C)中穿过NGC组织的线是来自组织处理的伪影。比例尺代表25 µm。

图6.A)每组4到6只动物,获得20 µm冰冻切片,并对脯氨酰4-羟化酶β(P4HB,红色)和神经丝200(NF200,绿色)染色。荧光显微照片显示了接受普通NGC的动物的代表性切片。导管用虚线白线表示。NF200+轴突和导管之间是一层P4HB+细胞,可能是由于异物反应引起的。一些细胞已经迁移到导管中(箭头)。B)同样,该区域包含CD68+巨噬细胞(红色),再次表明有异物反应。C)每组6到8只动物,组织用四氧化锇染色。得到0.7μm厚的切片,并用甲苯胺蓝复染。显微照片显示了接受普通NGC的动物的代表性切片。存在于导管内(左上角)和假定异物反应的P4HB+细胞层内(图像的其余部分)的似乎是含有大液泡(箭头)的细胞。比例尺代表(A,B)为100 µm,(C)为20 µm。
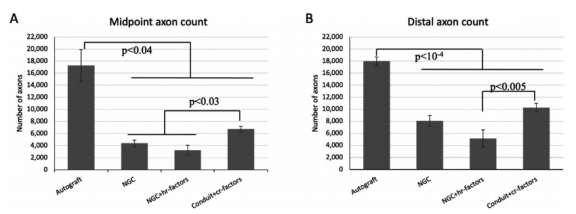
图7.有髓鞘轴突的计数。对于获得半薄切片的动物,使用立体学方法测量每个移植物或导管中有髓鞘轴突的数量。数据表示为平均值±平均值的标准偏差。A)从自体移植物或NGC的中点获得的有髓鞘轴突的计数。自体移植中有髓鞘轴突的数量明显高于任何一种NGC(p<0.04)。NGC+cr因子组的轴突计数显著高于其他两个NGC(p<0.03)。B)从远端神经获得的有髓鞘轴突的计数。自体移植组的有髓鞘轴突数量再次显著高于NGC组(p<10-4),而NGC+cr因子组高于NGC+hr因子组(p<0.005)。
