据WHO统计,心血管疾病是目前全球致死率最高的疾病,每年因心血管疾病死亡的人数超过1750万。目前,心血管疾病临床治疗有效方式之一是动脉搭桥术。但该治疗方式严重依赖自体血管移植,且易诱发一系列并发症,由此,心血管疾病治疗仍面临巨大挑战。近年来,随着新材料与组织工程的迅速发展,人工血管构建有望成为未来新的心血管疾病治疗方式。然而,如何成功实现血管内皮化,避免植入后发生血栓性栓塞乃至失效,仍是人工血管构建的一大难题。
近日,中国科学院深圳先进技术研究院的杜学敏副研究员及其团队设计了一种可从二维到三维自卷曲闭合的仿生小口径血管支架,并成功实现小口径血管的快速三维内皮化。相关研究成果发表在材料领域权威期刊Advanced Functional Materials 上,论文的第一作者为先进院的赵启龙博士,通讯作者为杜学敏副研究员。
杜学敏博士研究团队创新性地将仿生智能材料用于人工血管构建中来。基于前期在材料三维可控形变的设计(Advanced Materials, 2017, 29, 1702231)与利用外场(NIR)触发功能化植入柔性电子自适应形变成功的经验(Advanced Materials Technologies, 2017, 2, 1700120),他们结合形状记忆材料和静电纺丝技术,成功设计并构建了一种具有双层结构的新型仿生小口径血管支架。利用形状记忆材料独特的形状记忆特性,他们成功实现了平面薄膜支架在生理温度(37 °C)触发下,从临时二维薄膜形态转变为终态三维微管形状,从而实现了人工血管塑形。

图1. 平面薄膜支架在生理温度(37 °C)的触发下,从临时二维薄膜形态转变为终态三维微管形状
该研究团队进一步通过在形状记忆薄膜内面设计一层促细胞粘附的静电纺丝层,实现了血管内皮细胞在平面复合支架上均匀、稳固的黏附;同时,在塑形层的作用下,实现了小口径血管支架内腔三维仿生细胞的排布。研究发现,血管内皮细胞在可形变血管支架内经三维培养后可形成高度类似血管内膜组织结构的完备血管内皮细胞单层。
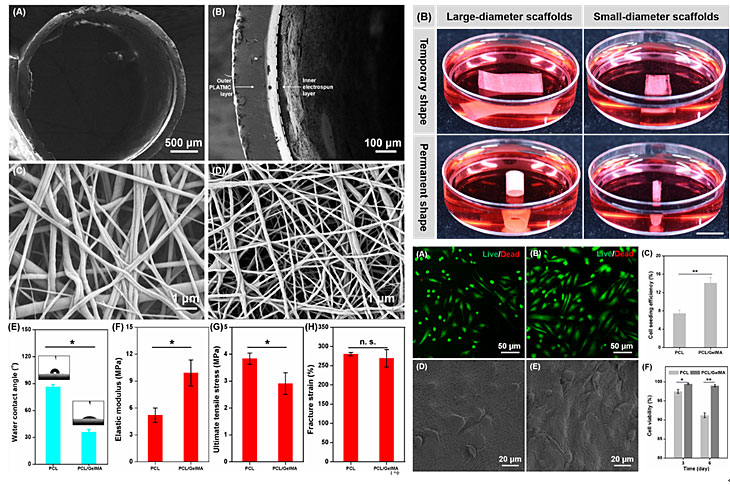
图2. 微管支架形貌图与力学分析(左);支架从临时二维薄膜形态转变为终态三维微管形状及其生物相容性分析(右)
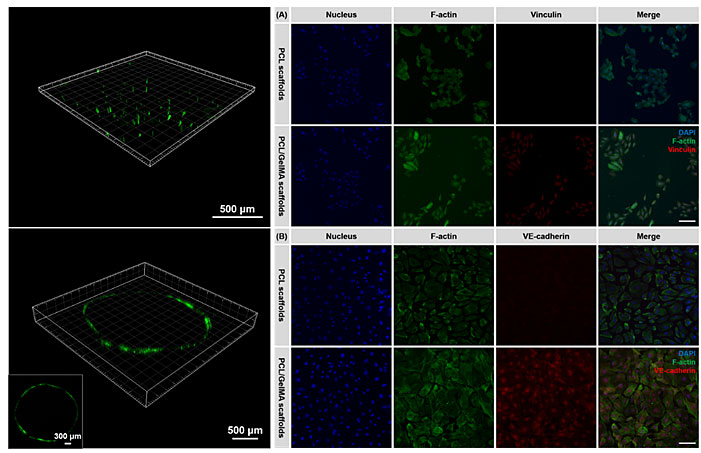
图3. 血管内皮细胞三维培养和内皮化
相关成果不仅为快速内皮化人工血管的构建提供了新的途径,而且也有望实现仿生血管内膜体外模型的构建及进一步用于心血管疾病治疗药物的筛选。更重要的是,该研究发展的基于仿生智能材料组织工程的构建方法也有望作为一种普适性的策略,推广并用于构建其他复杂结构的人造组织和器官。
论文全文链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.201801027
