导语
近日,中山大学欧阳钢锋教授、武汉大学黄卫华教授以及莱斯大学Kevin J. McHugh教授团队,分别在《Nature Water》、《Nature Communications》和《Nature Nanotechnology》上发表了关于纳米纤维的重要研究成果。易丝帮精选这三项高水平研究,带您快速了解纳米纤维在高效光催化膜、生物传感器及生物医用水凝胶等方面的最新突破与应用前景。
1、中山大学欧阳钢锋&叶宇昕Nature Water ( IF 24.1 ):在低光强度下进行高效水消毒的光催化膜


➣挑战:获得微生物安全的水仍然是一个紧迫的全球问题,特别是在资源有限和受灾害影响的地区。
➣方法:中山大学欧阳钢锋(国家杰青)、叶宇昕(国家优青)将 Cz-AQ 负载于 PS/PAN 混合纤维中,通过静电纺丝制备自漂浮、轻便、可裁剪的 PF-Cz-AQ 光催化薄膜。
➣创新点1:在低自然光照强度(13-18 mW cm−2)下,在10升高污染水中,40分钟内实现>4.3 log的细菌灭活,而传统光催化剂(如TiO2、g-C3N4等)几乎无效。这种卓越的性能归功于活性氧,尤其是以氧为中心的有机自由基,这是一种具有超长寿命的非常规活性物质,比典型的活性氧长几个数量级。它们的持久性允许在弱光照下积累,尽管光子输入有限,但仍保持消毒效率。
➣创新点2:此外,以氧为中心的有机自由基可以避免攻击催化剂,赋予优异的膜稳定性(可重复使用≥50次),从而确保成本效益和可持续性。
➣创新点3:这种光催化膜具有低能耗、高稳健性和操作简单的特点,特别适用于资源有限的地区,并有望在全球水安全的实际应用中得到应用。
http://doi.org/10.1038/s44221-025-00500-0
2、莱斯大学Kevin J. McHugh等人Nature Nanotechnology ( IF 34.9 ):纳米纤维超分子肽水凝胶

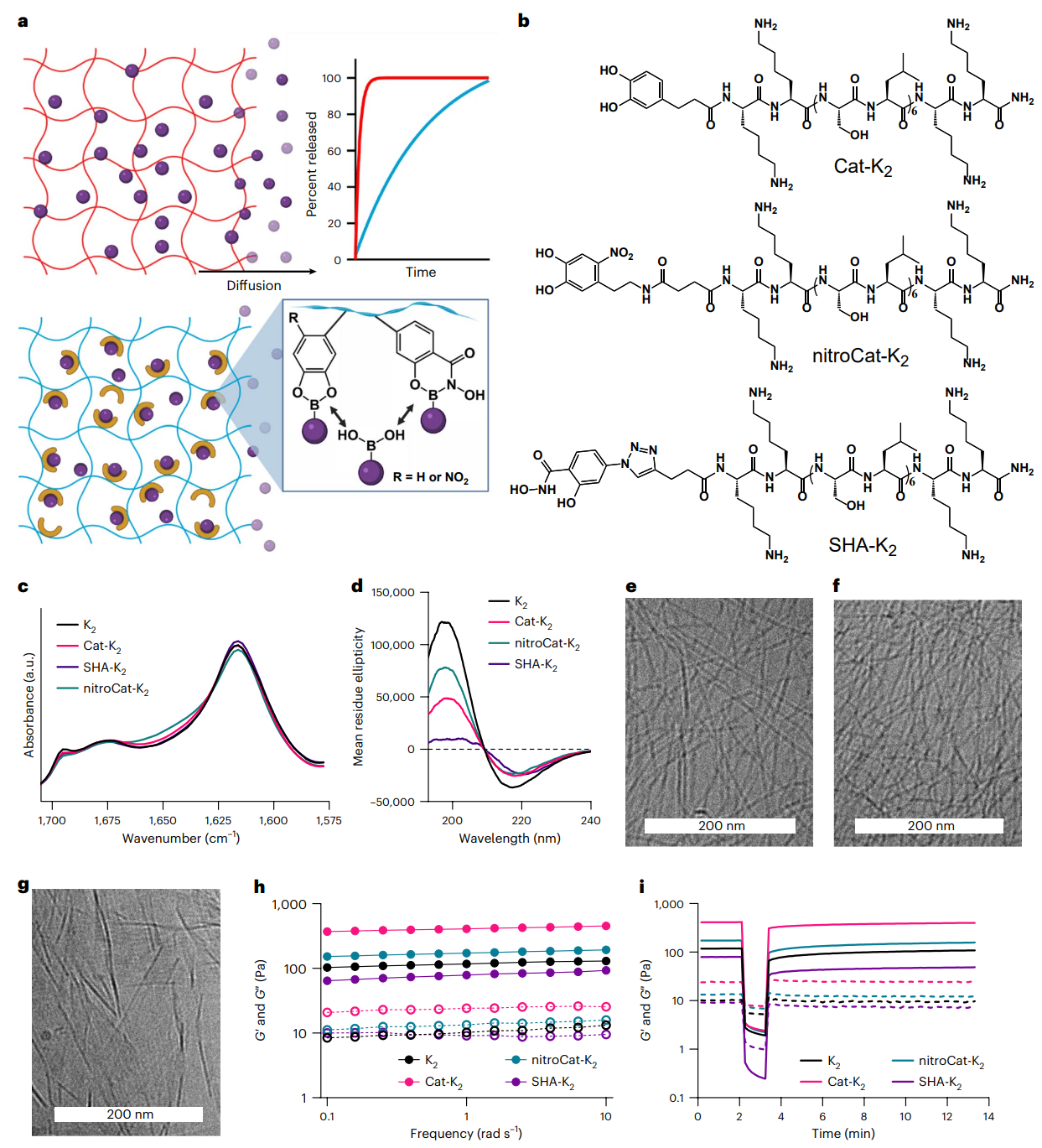
➣挑战:在体内维持安全和有效的药物水平是具有挑战性的。多结构域肽组装成具有良好定义的高多孔纳米结构的超分子水凝胶,这使得它们对药物输送具有吸引力。然而,它们延长释放的能力通常受到药物快速扩散的限制。
➣方法:莱斯大学Kevin J. McHugh和Jeffrey D. Hartgerink合作,开发了一种基于动态共价键的自组装硼酸酯释放(SABER)系统,通过在多域肽上引入4-硝基邻苯二酚或水杨基羟肟酸(SHA)等官能团,使其能与含硼酸(BA)的负载药物形成可逆共价键,显著延长药物释放时间。
➣创新点1:药代动力学研究表明,在感染模型中,与口服给药相比,SABER纳米纤维水凝胶可以将甘替博罗的治疗效果从几天延长到几周,防止结核分枝杆菌的生长。
➣创新点2:SABER纳米纤维水凝胶延长了胰岛素活性,单次注射后糖尿病小鼠血糖维持正常6天。这些结果表明SABER水凝胶具有广泛的临床转化潜力。
http://doi.org/10.1038/s41565-025-01981-6
3、武汉大学黄卫华教授&刘艳玲教授Nature Communications ( IF 15.7 ):同时用于机械刺激和电化学检测的磁响应纳米生物传感器

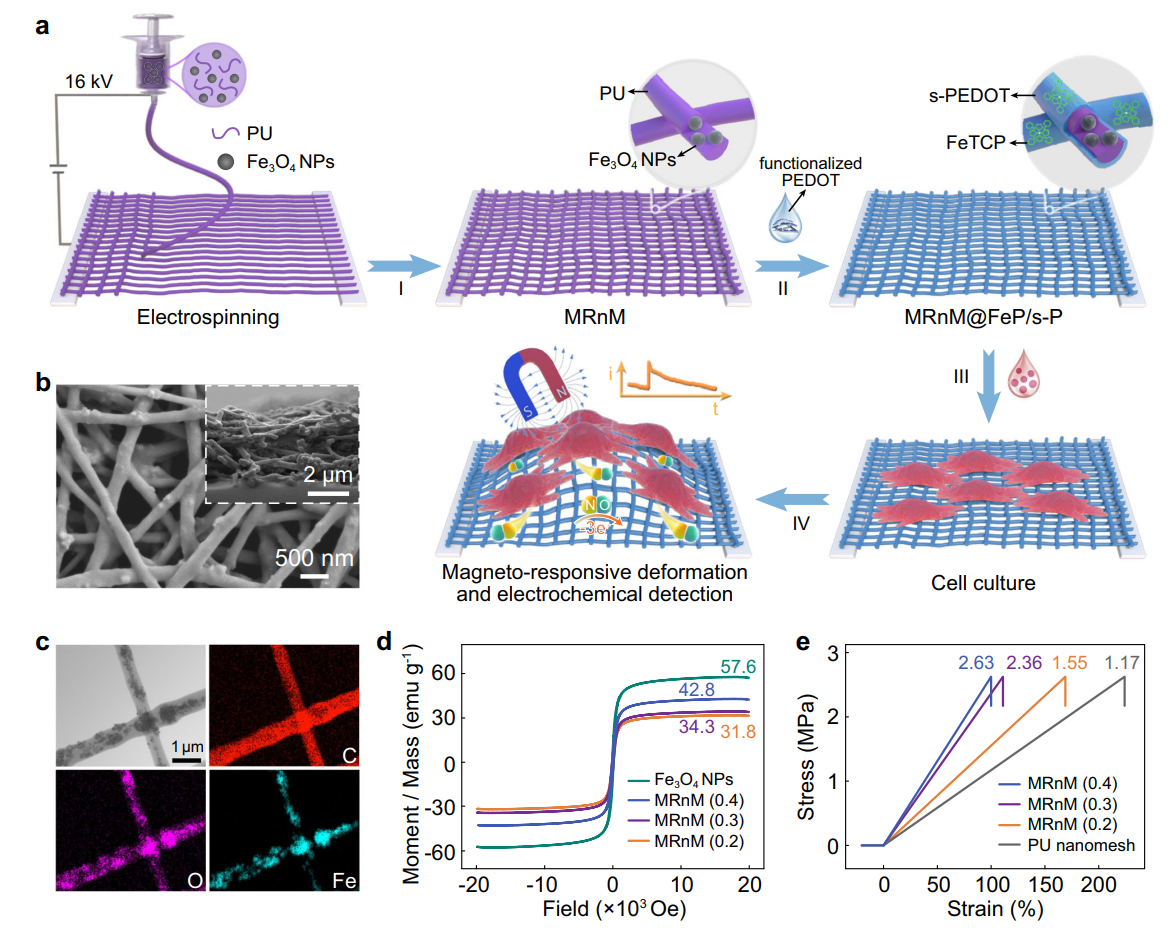
➣挑战:机械信号是细胞命运和行为的关键调节器,通过精心策划和持续的物理力量转化为生化反应。然而,由于机械和生化技术的兼容性差,现有的方法在表征机械刺激过程中发生的生化信号时往往受到限制。
➣方法:武汉大学黄卫华教授、刘艳玲教授团队采用静电纺丝将PU和Fe3O4纳米粒子(Fe3O4 NPs)溶液制成自支撑PU/Fe3O4纳米网,提出一种磁响应纳米(MRnM)生物传感器,能够机械刺激体外细胞和体内组织,同时检测被触发的生物分子。
➣创新点1:在外加磁场作用下,该传感器表现出优异的磁响应能力,可实现远程、可控和定制化变形,同时保持突出稳定的电化学传感性能。
➣创新点2:作为概念验证,该MRnM传感器实现了成骨细胞的磁致变形和随后的一氧化氮释放的实时监测,揭示了Piezo1通道在一氧化氮合酶信号通路中的作用。此外,还展示了MRnM传感器在体内应用的能力。
http://doi.org/10.1038/s41467-025-63623-8
