冰因其极滑的表面和极低的摩擦系数(COF)而广受认可。据报道,数百年前,它的超润滑表面(SLS)在中国古代曾被用于运输重型建筑材料。冰上的SLS归因于冰表面上固有的液态水层,并具有一定的稳定性。1961年, Hosler等证明该液态水层的厚度可以抵消冰表面的粗糙度,使其更光滑,从而改善其润滑性能。
生物医学膜在引导骨再生(GBR)、血液透析和抗组织粘附方面具有卓越的性能,因此已被广泛用于临床诊断、治疗和修复。这些生物膜通常需要足够的机械性能在履行特定生物学职能的同时保持完整性;通过电纺制备的纳米纤维膜是研究最频繁的抗粘附膜,因为它们的微/纳米多孔结构允许高渗透性和养分传输。膜的相互连接的微孔结构使其在摩擦时易于撕裂。由于其相对疏水的表面,大多数电纺膜都可以促进细胞粘附,该表面吸引了来自培养基或细胞分泌的细胞粘附蛋白。因此,在不使用药物的情况下,电纺纤维膜具有抗摩擦和细胞粘附的特性,同时保持孔隙率和力学性能是一种理想的方法。
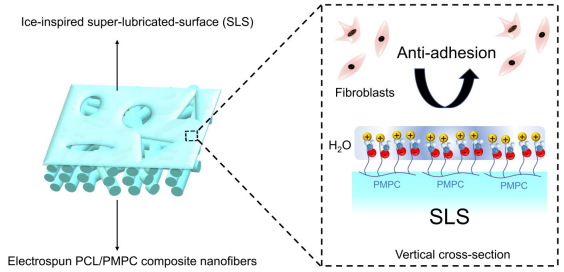
近日,清华大学张洪玉&上海交大瑞金医院崔文国&约翰霍普金斯大学毛海泉团队受冰的超润滑表面(SLS)的启发,在可控相对湿度(RH)下通过静电纺丝在聚己内酯(PCL)/聚(2-甲基丙烯酰氧基乙基磷酰胆碱)(PMPC)复合纳米纤维膜上构建了一个超润滑表面(SLS),该表面由超薄且连续的表面束缚水层组成。纳米纤维上的两性离子PMPC赋予了结合水表面层,从而产生了水合润滑表面。在20%RH下制备的电纺PCL/PMPC纳米纤维在PMPC与PCL的重量比为0.1时达到约0.12的最小摩擦系数(COF)。在较高的相对湿度下,在复合纳米纤维上形成了COF小于0.05的SLS。工程纳米纤维膜上SLS水化层的高稳定性有效抑制了成纤维细胞的粘附,并显著降低了肌腱在体内修复过程中的组织粘附。这项工作证明了这种受冰启发的SLS方法在预防组织粘连中的巨大潜力。 相关研究成果以“Ice-Inspired Super-Lubricated Electrospun Nanofibrous Membrane for Preventing Tissue Adhesion”为题目发表于国际期刊《Nano Letters》上。
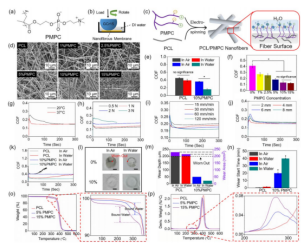
图1.(a)具有两性离子侧链的PMPC的结构。(b)摩擦学测试的示意图。(c)说明复合纳米纤维的独特结构。(d)具有变化的PMPC含量的不同电纺纤维膜的代表性SEM图像。(e)分别在空气和水中的PCL和10%PMPC样品的COF。(f–j)(f)PMPC含量,(g)温度,(h)正常负载,(i)转速和(j)旋转半径对样品的COF的影响。*p<0.05。(k)在空气和水中的PCL和10%PMPC样品的实测COF值随时间变化。(l)在空气和水中进行摩擦测量后,自然干燥的PCL和10%PMPC膜的图像。比例尺:2毫米。(m)PCL和10%PMPC组的磨损深度和(n)磨损开始时间。与PCL组相比,*p<0.05。(o)PCL、5%PMPC和15%PMPC样品的TGA和(p)DTG曲线。虚线框显示相应曲线的放大区域。
PCL/PMPC复合纳米纤维的摩擦学测试
为了确定PCL / PMPC复合纳米纤维膜的表面润滑性能(图1e-1n),进行了摩擦学测试。在往复模式下测试时,电纺膜很容易撕开,因此使用旋转测试模式,如图1b所示。从图1e中可以看出,加水可显着降低PCL/PMPC复合膜的COF,而与PCL纤维的COF没有明显区别。而且,PCL膜在空气中迅速磨损,尽管磨损面积较小(图1k,1l和1m),但最终在水下也磨损了。当纳米纤维中PMPC含量增加到5%以上时,复合膜的COF逐渐降低,并且显着低于纯PCL膜,当PMPC含量增加到10%时,COF最低达到约0.12(图1f)。在摩擦测试下,10%PMPC组在空气和水中都更稳定,几乎没有磨损(图1k和1l),同时水中的磨损深度比在空气中的磨损深度低(图1m)。在空气和水中,10%PMPC组开始显示出比PCL组更晚的磨损迹象(图1n)。 这些结果表明,纳米纤维上的PMPC表面层赋予纤维膜水化润滑性能,从而具有更好的耐磨性。
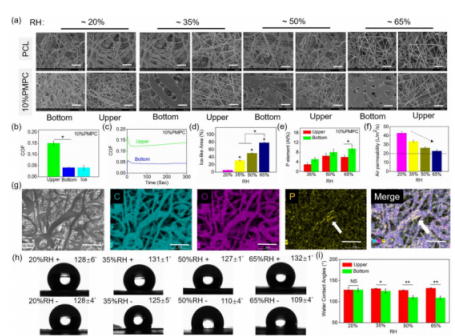
图2.(a)在不同相对湿度(RH)下制备的PCL和10%PMPC膜的代表性SEM图像。比例尺:10μm。底部:膜表面靠近铝箔。上部:相对的膜表面暴露在空气中。(b)65%RH样品的上、下表面以及冰面的COF。冰的COF来自先前的报告(6)。(c)10%PMPC膜的上表面和下表面的COF随时间变化。(d)从相应的SEM图像测得的SLS面积百分比。(e)35%RH、50%RH和65%RH10%PMPC样品的上表面和下表面的P元素含量(%)。(f)35%RH、50%RH和65%RH10%PMPC样品的透气率。(g)在35%RH下10%PMPC膜的底表面的二次电子/背散射电子图像。比例尺:30μm。(h)不同电纺纳米纤维的图像和(i)水接触角值。+:上,-:下。NS:无显著性。*p<0.05,**p<0.005。
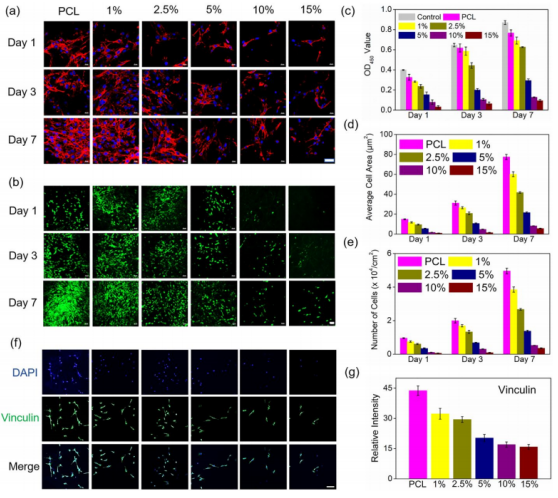
图3.PCL和具有不同PMPC含量的PCL/PMPC复合纳米纤维的(a)细胞骨架染色,(b)活/死染色和(f)纽蛋白免疫荧光染色的代表性CLSM图像。(c)基于CCK-8测定,不同天在450nm处的OD值。(d)从CLSM图像测得的平均细胞面积,(e)细胞数量和(g)相对强度。比例尺:(a)20μm,(b)50μm,和(f)20μm。
将NIH / 3T3成纤维细胞接种在电纺PCL / PMPC复合纤维膜和纯PCL膜上,以评估第1、3和7天的细胞黏附和增殖。使用鬼笔环肽(红色)和DAPI(蓝色)染色来可视化细胞骨架和细胞核通过共聚焦激光扫描显微镜(CLSM)分别在不同的膜表面上(图3a)。可以看出,细胞在PCL膜的表面扩散良好。
为了进一步评估细胞的黏附深度,我们使用了免疫荧光染色来检测粘连蛋白,一种典型的黏附相关蛋白。染色图像和相对表达分别显示在图3f和3g中。显然,长春花素在细胞边缘的丝状伪足和片状脂质体的终末纤维束中表达,在PCL,1%PMPC和2.5%PMPC组中显示出密集的点状绿色荧光。相比之下,在5%PMPC,10%PMPC和15%PMPC膜上几乎没有表达过蛋白结合信号。随着PMPC浓度的增加,纽蛋白表达逐渐降低,在15%PMPC膜中纽蛋白表达最低。在图3g中分析了平均荧光强度的半定量,并且与免疫荧光结果一致。
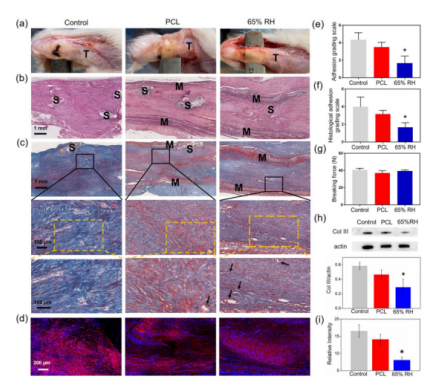
图4.(a)对照、PCL和65%RH/10%PMPC组第21天手术部位的宏观图像和(b)H&E染色图像。S:缝合部位,M:膜。(c)在第21天,对照组、PCL组和65%RH/10%PMPC组的Masson染色图像。黑框和黄色虚线框是相应区域的放大图像。黑色箭头指向可能新形成的血管。(d)在第21天,对照组、PCL和65%RH/10%PMPC组的Col III免疫荧光染色图像。红色代表Col III表达,蓝色代表成纤维细胞核。(e)粘附力分级量表,(f)组织学粘附力分级量表,(g)断裂力,(h)Col III的Western印迹数据,以及(i)对照、PCL和65%RH/10%PMPC组Col III的相对强度。与PCL组相比,*p<0.05。
论文链接:https://doi.org/ 10.1021/acs.nanolett.
